题目内容
16.可以充分说明反应P(g)+Q(g)?R(g)+S(g)在恒温下已达到平衡( )| A. | 反应容器内的压强不随时间改变 | |
| B. | 反应容器内P、Q、R、S四者共存 | |
| C. | P的生成速率和S的生成速率相等 | |
| D. | 反应容器内的气体总物质的量不随时间变化 |
分析 可逆反应达到平衡状态时,正逆反应速率相等,反应体系中各物质的量不变、物质的量浓度不变、百分含量不变以及由此引起的一系列物理量不变,据此分析解答.
解答 解:A.该反应前后气体物质的量之和不变,则压强始终不变,所以不能根据压强判断平衡状态,故A错误;
B.无论该反应是否达到平衡状态,反应容器中P、Q、R、S四者共存,所以不能据此判断平衡状态,故B错误;
C.P和S的生成速率相等,则P的消耗速率和生成速率相等,该反应达到平衡状态,故C正确;
D.无论反应是否达到平衡状态,反应容器中总的物质的量始终保持不变,不能据此判断平衡状态,故D错误;
故选C
点评 本题考查化学平衡状态判断,为高频考点,只有反应前后改变的物理量才能作为平衡状态判断依据,易错选项是A,为易错题.

练习册系列答案
相关题目
6.铝、钠混合物投入足量的水中,充分反应后,得到澄清溶液,并收集到4.48L氢气(标准状况),若钠的物质的量为0.1mol,则铝的物质的量为( )
| A. | 0.1mol | B. | 0.2mol | C. | 0.05mol | D. | 0.025mol |
7.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 2gH2中含有的分子数为NA | |
| B. | 标准状况下,22.4LH2O中含有的分子数为NA | |
| C. | 1mol/L K2SO4的溶液中含有钾离子数为2NA | |
| D. | 1mol钠原子中含有的电子数为NA |
4.食品干燥剂应无毒、无味、无腐蚀性及环境友好.下列说法错误的是( )
| A. | 硅胶可用作食品干燥剂 | |
| B. | 烧碱固体可用作食品干燥剂 | |
| C. | P2O5不可用作食品干燥剂 | |
| D. | 具有吸水性的植物纤维可用作食品干燥剂 |
1.下列粒子在化学反应中既能显示氧化性又能显示还原性的是( )
| A. | H+ | B. | Cl- | C. | Al | D. | Fe2+ |
8.下列化学方程式能用离子方程式H++OH-=H2O表示的是( )
| A. | 氢氧化铁和稀硝酸反应 | B. | 氢氧化钡和稀盐酸反应 | ||
| C. | 氢氧化钾溶液中通入硫化氢气体 | D. | 氢氧化钡溶液和稀硫酸反应 |
5.加成反应是有机化合物分子中双键上的碳原子与其他原子(或原子团)直接结合生成新的化合物分子的反应,下列过程与加成反应无关的是( )
| A. | 苯与溴水混合振荡,水层颜色变浅 | |
| B. | 裂化汽油与溴水混合振荡,水层颜色变浅 | |
| C. | 乙烯与水在一定条件下反应制取乙醇 | |
| D. | 乙烷与氯气在一定条件下反应制取的一氯乙烷 |
17.辉铜矿主要成分Cu2S,软锰矿主要成分MnO2,它们都含有少量SiO2、Fe2O3等杂质.工业上综合利用这两种矿物制备硫酸锰和碱式碳酸铜的主要工艺流程如下:
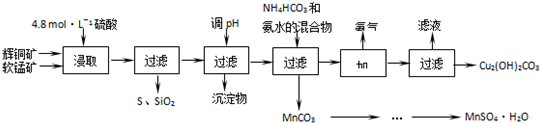
已知:①MnO2能将金属硫化物中的硫氧化为单质硫;②[Cu(NH3)4]SO4常温稳定,在热水中会分解生成NH3;③部分金属阳离子生成氢氧化物沉淀 的pH范围如下表所示
(1)酸浸时,为了提高浸取率可采取的措施有粉碎矿石(或适当升高温度或搅拌)(任写一点).
(2)酸浸时,得到的浸出液中主要含有CuSO4、MnSO4等.写出该反应的化学方程式2MnO2+Cu2S+4H2SO4=S+2CuSO4+2MnSO4+4H2O.
(3)调节浸出液pH的范围为3.2≤PH<4.4,其目的是使Fe3+离子转化为氢氧化铁沉淀除去.
(4)本工艺中可循环使用的物质是NH3(写化学式).
(5)用标准BaCl2溶液测定样品中MnSO4•H2O质量分数时,发现样品纯度大于100%(测定过程中产生的误差可忽略),其可能原因有混有硫酸盐杂质或部分晶体失去结晶水(任写一种).

已知:①MnO2能将金属硫化物中的硫氧化为单质硫;②[Cu(NH3)4]SO4常温稳定,在热水中会分解生成NH3;③部分金属阳离子生成氢氧化物沉淀 的pH范围如下表所示
| 开始沉淀的pH | 沉淀完全的pH | |
| Fe3+ | 1.1 | 3.2 |
| Mn2+ | 8.3 | 9.8 |
| Cu2+ | 4.4 | 6.4 |
(2)酸浸时,得到的浸出液中主要含有CuSO4、MnSO4等.写出该反应的化学方程式2MnO2+Cu2S+4H2SO4=S+2CuSO4+2MnSO4+4H2O.
(3)调节浸出液pH的范围为3.2≤PH<4.4,其目的是使Fe3+离子转化为氢氧化铁沉淀除去.
(4)本工艺中可循环使用的物质是NH3(写化学式).
(5)用标准BaCl2溶液测定样品中MnSO4•H2O质量分数时,发现样品纯度大于100%(测定过程中产生的误差可忽略),其可能原因有混有硫酸盐杂质或部分晶体失去结晶水(任写一种).
