题目内容
7.2015年7月31日,中国获得2022年冬奥会主办权,这将促进中国冰雪运动,以下关于冰的说法正确的是( )| A. | 冰与水共存物属于混合物 | B. | 冰的密度比水大 | ||
| C. | 冰与二氧化硅的晶体类型相似 | D. | 氢键在冰晶体结构中起关键作用 |
分析 A.冰与水的成分相同;
B.冰的密度小于水;
C.冰属于分子晶体;
D.氢键使晶体中分子排列更加有序.
解答 解:A.冰与水的成分相同,则冰与水共存物属于纯净物,故A错误;
B.冰晶体由于氢键的作用,使分子排列更加有序,分子间的距离增大,体积膨胀,密度减小,所以冰的密度小于水,故B错误;
C.冰属于分子晶体,二氧化硅属于原子晶体,则二者晶体类型不同,故C错误;
D.氢键使晶体中分子排列更加有序,则氢键在冰晶体结构中起关键作用,故D正确.
故选D.
点评 本题考查了混合物的概念、氢键、晶体的判断,侧重于基础知识的考查,题目难度不大.

练习册系列答案
相关题目
17.如图1为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题:
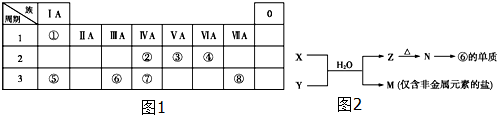
(1)写出由④、⑤、⑧元素形成的既含离子键又含共价键的一种离子化合物的化学式:NaClO.
(2)含元素⑧的单质能与自来水中的有机物反应生成对人体有危害的物质,现已逐步淘汰.下列可代替它作自来水消毒剂的是AC.
A.ClO2 B.AlCl3 C.K2FeO4
(3)W与④是相邻的同主族元素.在下表中写出H2WO3相应性质的化学方程式.
(4)由表中元素形成的常见物质X、Y、Z、M、N可发生如图2反应:
X溶液与Y溶液反应的离子方程式为Al3++3NH3+3H2O═Al(OH)3↓+3NH4+;
M中阳离子的鉴定方法是取少量M样品放入试管,加入氢氧化钠溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体,证明有铵根离子;
如果M中含有元素⑧,M溶液中离子浓度由大到小的排列顺序是c(Cl-)>c(NH+4)>c(H+)>c(OH-).

(1)写出由④、⑤、⑧元素形成的既含离子键又含共价键的一种离子化合物的化学式:NaClO.
(2)含元素⑧的单质能与自来水中的有机物反应生成对人体有危害的物质,现已逐步淘汰.下列可代替它作自来水消毒剂的是AC.
A.ClO2 B.AlCl3 C.K2FeO4
(3)W与④是相邻的同主族元素.在下表中写出H2WO3相应性质的化学方程式.
| 编号 | 性质 | 化学方程式 |
| 1 | 还原性 | H2SO3+Br2+2H2O═H2SO3+2HBr |
| 2 | 酸性 | H2SO3+2NaOH=Na2SO3+2H2O |
X溶液与Y溶液反应的离子方程式为Al3++3NH3+3H2O═Al(OH)3↓+3NH4+;
M中阳离子的鉴定方法是取少量M样品放入试管,加入氢氧化钠溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体,证明有铵根离子;
如果M中含有元素⑧,M溶液中离子浓度由大到小的排列顺序是c(Cl-)>c(NH+4)>c(H+)>c(OH-).
15.黄铁矿石的主要成分为FeS2和少量FeS(假设其他杂质中不含Fe、S元素,且高温下不发生化学变化),是我国大多数硫酸厂制取硫酸的主要原料.某化学兴趣小组对该黄铁矿石进行如下实验探究.将m1g该黄铁矿石的样品放入如图装置(夹持和加热装置略)的石英管中,从a处不断地缓缓通入空气,高温灼烧黄铁矿样品至反应完全.

其反应的化学方程式为:
4FeS2+11O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+8SO2
4FeS+7O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+4SO2
【实验一】:测定硫元素的含量反应结束后,将乙瓶中的溶液进行如下处理:
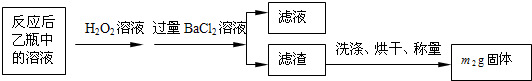
(1)鼓入空气的作用是提供反应需要的氧气,排出装置中生成的二氧化硫被乙装置全部吸收.
(2)反应结束后乙瓶中的溶液需加足量H2O2溶液的目的是Na2SO3+H2O2=Na2SO4+H2O(用化学方程式表示).
(3)该黄铁矿石中硫元素的质量分数为$\frac{32{m}_{2}}{233{m}_{1}}$×100%(列出表达式即可).
【实验二】:测定铁元素的含量
①用足量稀硫酸溶解石英管中的固体残渣→②加还原剂使溶液中的Fe3+恰好完全转化为Fe2+后,过滤、洗涤→③将滤液稀释至250mL→④取25.00mL稀释液用0.1 000mol/L的酸性KMnO4溶液滴定
(4)②中,若用铁粉作还原剂,则所测得的铁元素的含量偏大(填“偏大”、“偏小”或“无影响”).
(5)③中,需要用到的仪器除烧杯、玻璃棒、胶头滴管外,还有250mL容量瓶.
(6)某同学一共进行了四次滴定实验,实验结果记录如下:
根据所给数据,计算该稀释液中Fe2+的物质的量浓度为c(Fe2+)=0.5000mol/L.

其反应的化学方程式为:
4FeS2+11O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+8SO2
4FeS+7O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+4SO2
【实验一】:测定硫元素的含量反应结束后,将乙瓶中的溶液进行如下处理:

(1)鼓入空气的作用是提供反应需要的氧气,排出装置中生成的二氧化硫被乙装置全部吸收.
(2)反应结束后乙瓶中的溶液需加足量H2O2溶液的目的是Na2SO3+H2O2=Na2SO4+H2O(用化学方程式表示).
(3)该黄铁矿石中硫元素的质量分数为$\frac{32{m}_{2}}{233{m}_{1}}$×100%(列出表达式即可).
【实验二】:测定铁元素的含量
①用足量稀硫酸溶解石英管中的固体残渣→②加还原剂使溶液中的Fe3+恰好完全转化为Fe2+后,过滤、洗涤→③将滤液稀释至250mL→④取25.00mL稀释液用0.1 000mol/L的酸性KMnO4溶液滴定
(4)②中,若用铁粉作还原剂,则所测得的铁元素的含量偏大(填“偏大”、“偏小”或“无影响”).
(5)③中,需要用到的仪器除烧杯、玻璃棒、胶头滴管外,还有250mL容量瓶.
(6)某同学一共进行了四次滴定实验,实验结果记录如下:
| 实验次数 | 第一次 | 第二次 | 第三次 | 第四次 |
| 消耗KMnO4溶液体积/mL | 25.00 | 25.03 | 20.00 | 24.97 |
2.电动自行车由于灵活、快捷、方便,已成为上班族的主要代步工具,其电源常采用铅蓄电池,反应原理为PbO2+Pb+2H2SO4$?_{充电}^{放电}$2PbSO4+2H2O,下列叙述正确的是( )
| A. | 电池放电时,PbO2是电池的正极,被氧化 | |
| B. | 电池放电时,SO42-只在负极发生反应 | |
| C. | 电池充电时,溶液的pH不断增大 | |
| D. | 电池充电时,阳极反应式为PbSO4+2H2O-2e-═PbO2+SO42-+4H+ |
12.用NA表示阿伏伽德罗常数,下列叙述正确的是( )
| A. | 1mol甲基(-CH3)含有9NA个电子 | |
| B. | 标准状况下,22.4LSO3含有的原子数为4NA | |
| C. | 0.10mol•L-1NaOH溶液中含有OH1离子数是0.1NA | |
| D. | 5.6Fe与2.24LCl2充分反应转移电子数为0.2NA |
19.在一密闭容器中有如下反应:aX(g)+bY(g)?nW(g)△H=Q.某化学兴趣小组的同学根据此反应在不同条件下的实验数据,作出了如下曲线图:

其中,ω(W)表示W在反应混合物中的百分含量,t表示反应时间.其它条件不变时,下列分析可能正确的是( )

其中,ω(W)表示W在反应混合物中的百分含量,t表示反应时间.其它条件不变时,下列分析可能正确的是( )
| A. | 图Ⅰ可能是不同压强对反应的影响,且P2>P1,a+b<n | |
| B. | 图Ⅲ可能是不同温度对反应的影响,且T1>T2,Q<0 | |
| C. | 图Ⅱ可能是不同压强对反应的影响,且P1>P2,n<a+b | |
| D. | 图Ⅱ可能是在同温同压下催化剂对反应的影响,且2表示使用催化剂后的反应过程 |
16.下列溶液一定呈中性的是( )
| A. | pH=7的溶液 | |
| B. | c(OH-)=$\sqrt{{K}_{W}}$ | |
| C. | 由强酸与强碱等物质的量反应得到的溶液 | |
| D. | 强电解质溶于水得到的溶液 |
17.下列性质不属于甲烷性质的是( )
| A. | 完全燃烧时生成CO2和H2O | |
| B. | 常温常压下能溶于水 | |
| C. | 光照下能与卤素单质发生取代反应 | |
| D. | 通常情况下,跟强酸、强碱和强氧化剂不反应 |
 、
、 ,该反应的化学方程式为:2CO2+Na2O2═2Na2CO3+O2.
,该反应的化学方程式为:2CO2+Na2O2═2Na2CO3+O2.