题目内容
下列离子方程式正确的是( )
| A、碳酸钡与盐酸反应:2H++BaCO3=Ba2++H2O+CO2↑ |
| B、氢氧化钡溶液与稀硫酸混合:Ba2++SO42-+H++OH-=BaSO4↓+H2O |
| C、氯气通入蒸馏水中:Cl2+H2O=Cl-+ClO-+2H+ |
| D、CO2通入过量的澄清石灰水中:CO2+Ca(OH)2=CaCO3↓+H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A.反应生成氯化钡、水、二氧化碳;
B.不符合离子的配比;
C.HClO在离子反应中保留化学式;
D.过量的澄清石灰水,反应生成碳酸钙和水,氢氧化钙应完全电离.
B.不符合离子的配比;
C.HClO在离子反应中保留化学式;
D.过量的澄清石灰水,反应生成碳酸钙和水,氢氧化钙应完全电离.
解答:
解:A.碳酸钡与盐酸反应的离子反应为2H++BaCO3=Ba2++H2O+CO2↑,故A正确;
B.氢氧化钡溶液与稀硫酸混合的离子反应为Ba2++SO42-+2H++2OH-=BaSO4↓+2H2O,故B错误;
C.氯气通入蒸馏水中的离子反应为Cl2+H2O=Cl-+HClO+H+,故C错误;
D.CO2通入过量的澄清石灰水中的离子反应为CO2+Ca2++2OH-=CaCO3↓+H2O,故D错误;
故选A.
B.氢氧化钡溶液与稀硫酸混合的离子反应为Ba2++SO42-+2H++2OH-=BaSO4↓+2H2O,故B错误;
C.氯气通入蒸馏水中的离子反应为Cl2+H2O=Cl-+HClO+H+,故C错误;
D.CO2通入过量的澄清石灰水中的离子反应为CO2+Ca2++2OH-=CaCO3↓+H2O,故D错误;
故选A.
点评:本题考查离子反应书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重复分解反应的离子反应考查,注意离子反应中保留化学式的物质,题目难度不大.

练习册系列答案
 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案
相关题目
对以下化学问题的解释中错误的是( )
| A、工业盐酸显黄色,是由于含有杂质FeCl3 |
| B、碘化钾溶液久置显黄色,是由于I被氧化,析出的I2溶于溶液中 |
| C、浓硝酸显黄色,是由于硝酸见光分解生成的NO2溶液酸液中 |
| D、炼钢是在高温下利用还原剂除去生铁中的杂质 |
对于反应14CuSO4+5FeS2+12H2O═7Cu2S+5FeSO4+12H2SO4来说,下列结论正确的是( )
| A、FeS2既是氧化剂,又是还原剂 |
| B、只有CuSO4作氧化剂 |
| C、被氧化的硫和被还原的硫质量比是3:7 |
| D、被氧化的硫和被还原的硫质量比是1:1 |
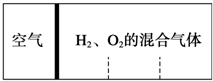 如图所示,分别向密闭容器内可移动活塞的两边充入空气(已知空气体积占整个容器容积的
如图所示,分别向密闭容器内可移动活塞的两边充入空气(已知空气体积占整个容器容积的| 1 |
| 4 |
| A、2:7 | B、5:4 |
| C、2:1 | D、4:5 |
设NA为阿伏加德罗常数的值,下列说法正确的组合是( )
| A、常温下,1mol/L的NH4NO3溶液中含有氮原子的数目为2NA |
| B、17g H2O2中含有的电子数为9NA |
| C、将2mol SO2与1mol O2混合,发生反应转移的电子总数一定是4NA |
| D、常温下,100mL 1mol?L-1 AlCl3溶液中铝离子数为0.1NA |
下列叙述正确的是( )
| A、元素处于最高价态时一定有强氧化性;同理元素处于最低价态时一定具有强还原性 |
| B、将FeCl2溶液与稀HNO3混合离子反应方程式:Fe2++4H++NO3-═Fe3++NO↑+2H2O |
| C、HF、Al(OH)3、氨水都是弱电解质 |
| D、颜色反应、显色反应、指示剂变色反应均属化学变化 |
下列各表述与示意图一致的是( )
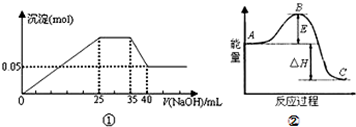

| A、图①表示向含Mg2+、Al3+、NH4+的盐溶液中滴加NaOH溶液时,沉淀的量与NaOH的体积的关系图.则三种离子的物质的量之比为:n(Mg2+):n(Al3+):n( NH4+)=2:1:2 |
| B、图①中使用的NaOH的浓度为2mol?L-1 |
| C、图②中物质A反应生成物质C,△H>0 |
| D、图②中曲线表示某反应过程的能量变化,若使用催化剂,E值会减小 |
已知25℃时有关弱酸的电离平衡常数如下.下列有关说法正确的是( )
| 弱酸化学式 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | 1.8×10-5 | 4.9×l0-10 | K1=4.3×10-7 K2=5.6×10-11 |
| A、NaHCO3溶液中,一定有c(Na+)=c(HCO3-)+c(CO32-) |
| B、将a mol?L-1HCN溶液与a mol?L-1 NaOH溶液等体积混合后,测得所得溶液显碱性(pH>7),则c(OH-)>c(H+),c(CN-)>c(Na+) |
| C、等物质的量浓度的各溶液pH关系为:pH(Na2CO3)>pH(NaCN)>pH(CH3COONa) |
| D、1mol/L醋酸溶液加水稀释,溶液中所有离子浓度均减小 |