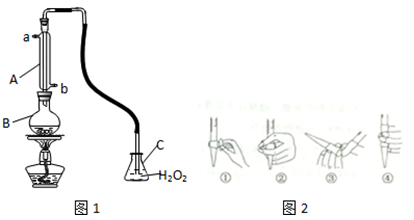
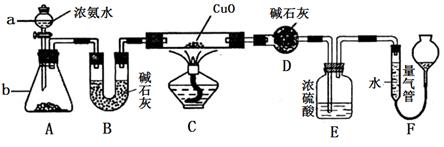
题目内容
三氯异氰尿酸(结构简式如图)是一种极强的氧化剂和氯化剂。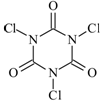
(1)利用三氯异氰尿酸水解产物中的氧化性物质X可消毒灭菌,X的分子式为 。
(2)“有效氯”含量指从KI中氧化出相同量的I2所需Cl2的质量与指定化合物的质量之比,常以百分数表示。为测定三氯异氰尿酸的“有效氯”含量,现称取某三氯异氰尿酸样品0.5680 g,加水、足量KI、硫酸,配制成100 mL待测液;准确量取25.00 mL待测液于碘量瓶中,用0.1500 mol·L-1 Na2S2O3标准溶液滴定至溶液呈微黄色时,加入淀粉指示剂,继续滴定至终点(发生反应的方程式为:2Na2S2O3+I2=Na2S4O6+2NaI);重复测定2次,所得的相关数据如下表:
| 滴定序号 | 待测液体积/mL | 标准液滴定管起点读数/mL | 标准液滴定管终点读数/mL |
| 1 | 25.00 | 0.06 | 24.04 |
| 2 | 25.00 | 0.02 | 24.02 |
| 3 | 25.00 | 0.12 | 24.14 |
①滴定终点观察到的现象为 ;
②配制0.1500 mol·L-1 Na2S2O3溶液100 mL,所需Na2S2O3·5H2O的质量为 ;
③计算此样品的“有效氯”含量(写出计算过程)。
(1)HClO(2分)
(2)①溶液蓝色褪去,且30 s内不变色(2分)
②3.72 g(2分)
③3次消耗标准Na2S2O3溶液的平均值为24.00 mL(1分)
根据反应:
Cl2+2I-=2Cl-+I2,2Na2S2O3+I2=Na2S4O6+2NaI 知:
n(Cl2)=4×(1/2×0.1500 mol·L-1×24.00×10-3 L) =7.2×10-3 mol(2分)
m(Cl2)=7.2×10-3 mol×71 g·mol-1=0.5112 g(2分)
解析试题分析:(1)三氯异氰尿酸中氯原子水解,氯原子结合羟基,生成HClO,其具有强氧化性;(2)①碘溶液加入淀粉为蓝色,终点时溶液蓝色褪去,且30 s内不变色;
②所需Na2S2O3·5H2O的质量为0.1500 ×0.1×248="3.72" g
③3次消耗标准Na2S2O3溶液的平均值为24.00 mL
根据反应:Cl2+2I-=2Cl-+I2,2Na2S2O3+I2=Na2S4O6+2NaI
确定关系式Cl2——I2——2Na2S2O3
n(Cl2)=4×(1/2×0.1500 mol·L-1×24.00×10-3 L) =7.2×10-3 mol(2分)
m(Cl2)=7.2×10-3 mol×71 g·mol-1=0.5112 g(2分)
考点:考查工业定量实验中数据的测定的方法及计算有关问题。

下列各组中的实验步骤及现象,能达到相应实验目的的是
| | 实验目的 | 实验步骤及现象 |
| A | 检验亚硫酸钠试样是否变质 | 试样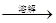  白色沉淀 白色沉淀 沉淀不溶解 沉淀不溶解 |
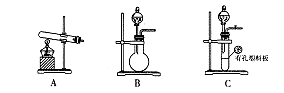
| B | 制取氯气并探究氯气是否具有漂白性 | MnO2和稀盐酸 气体 气体 褪色 褪色 |
| C | 证明酸性条件H2O2氧化性比I2强 | 碘化钠溶液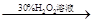 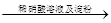 溶液变蓝色 溶液变蓝色 |
| D | 探究浓度对于化学平衡的影响 | FeCl3和KSCN混合溶液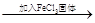 红色变深 红色变深 |
下列有关实验操作的叙述正确的是
| A.配制FeCl3溶液时,将FeCl3溶解在较浓的盐酸中,再用水稀释到所需浓度 |
| B.进行焰色反应时,所用铂丝先用NaOH溶液洗涤并充分灼烧 |
| C.用CCl4萃取碘水中的I2时,有机层从分液漏斗的上端倒出 |
| D.酸碱中和滴定时,锥形瓶需用待测液润洗2次,再加入待测液 |
下列实验不能达到目的的是
| A.用AlCl3溶液和过量氨水制备Al(OH)3 |
| B.用NH4Cl和Ca(OH) 2固体混合加热制备NH3 |
| C.用NaOH溶液除去苯中的溴 |
| D.用足量铜粉除去FeCl2溶液中的FeCl3杂质 |
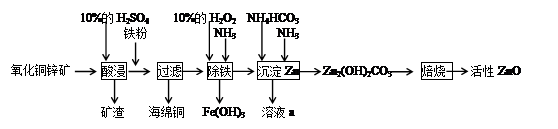
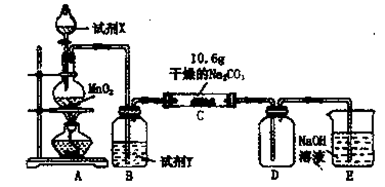
 (3)已知C中有0.1 mol Cl2参加反应。若假设一成立,可推知C中反应的化学方程式为 。
(3)已知C中有0.1 mol Cl2参加反应。若假设一成立,可推知C中反应的化学方程式为 。