题目内容
【题目】某温度下,在一个2L的密闭容器中,发生反应3A(g)+2B(g)![]() 4C(s)+2D(g),加入4molA和2molB,2min后达到平衡,测得生成1.6mol C,则下列说法正确的是:
4C(s)+2D(g),加入4molA和2molB,2min后达到平衡,测得生成1.6mol C,则下列说法正确的是:
A.该反应的化学平衡常数表达式是K=![]()
B.此时,B的平衡转化率是40%
C.增大该体系的压强,平衡向右移动,化学平衡常数增大
D.若向平衡体系移走部分D,则此时正反应速率增大
【答案】B
【解析】
A. 依据平衡常数的概念分析列式得到,C为固体不写入平衡常数的表达式,K=![]() ,A项错误;
,A项错误;
B. 依据平衡三段式列式计算;加入4molA和2molB进行反应,反应一段时间后达到平衡,测得生成1.6molC,则
3A(g)+2B(g)![]() 4C(s)+2D(g)
4C(s)+2D(g)
起始量(mol) 4 2 0 0
转化量(mol) 1.2 0.8 1.6 0.8
平衡量(mol) 2.8 1.2 1.6 0.8
则B的转化率![]() ,B项正确;
,B项正确;
C. 反应后气体体积减小,增大压强平衡正向进行,但平衡常数只与温度有关,压强变化平衡常数不变,C项错误;
D. 若向平衡体系移走部分D,则此时正反应的反应物浓度瞬间不变,故正反应速率瞬间并未变化,然后随着反应的进行,正反应速率减慢,D项错误;
答案选B。

练习册系列答案
相关题目
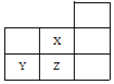
【题目】如图是元素周期表的一部分:
数据编号 | 滴入NaOH溶液的体积 | 溶液的pH | |
HX | HZ | ||
1 | 0 | 3 | 1 |
2 |
| a | b |
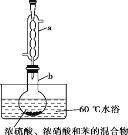
![]() 时,用浓度为
时,用浓度为![]() 的氢氧化钠溶液分别滴定
的氢氧化钠溶液分别滴定![]() 浓度均为
浓度均为![]() 的两种酸HX、
的两种酸HX、![]() 忽略体积变化
忽略体积变化![]() ,实验数据如表2,下列判断正确的是
,实验数据如表2,下列判断正确的是![]()
A.通过分析可得表格中![]() ,
,![]()
B.将上述的HZ溶液稀释100倍后pH比HX溶液的pH大
C.由于Z元素的非金属性比Y强,所以Z氢化物的酸性较强
D.![]()
![]()
![]() 的水溶液中:
的水溶液中:![]()
![]()