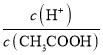题目内容
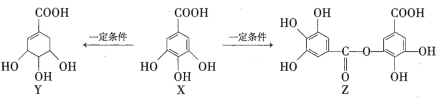
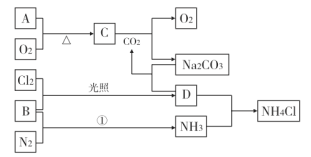
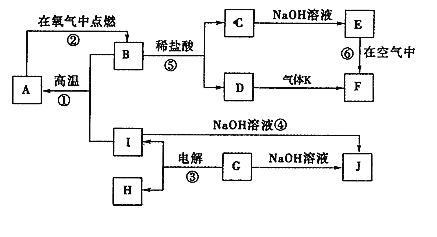
【题目】有机物G是一种医药中间体,可通过如图所示路线合成。A是石油化工的重要产品且分子中所有原子在同一平面内,H的分子式是C7H8。
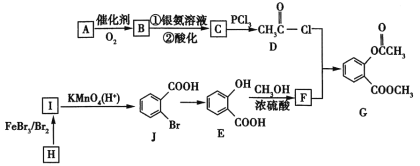
已知:![]() 。
。
回答下列问题。
(1)A的结构简式是___________。
(2)H→I的化学方程式为__________,B与银氨溶液反应的化学方程式是__________。
(3)C→D的反应类型是______,I→J的反应类型是______。
(4)两个E分子在一定条件下发生分子间脱水生成一种环状酯的结构简式是_______________。
(5)满足以下条件的F的同分异构体(不含F)共有_________种。
①能与氯化铁溶液发生显色反应 ②分子中有—COO—结构 ③苯环上有两个取代基
【答案】CH2=CH2 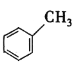 +Br2
+Br2![]()
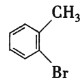 +HBr
+HBr ![]() 取代反应 氧化反应
取代反应 氧化反应 ![]() 11
11
【解析】
A是石油化工的重要产品且分子中所有原子在同一平面内,结合D的结构简式可知A为CH2=CH2,由转化关系可知,B为CH3CHO,C为CH3COOH,结合G的结构简式可知,F为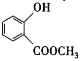 ,H的分子式是C7H8,不饱和度为4,H含有一个苯环,故H为
,H的分子式是C7H8,不饱和度为4,H含有一个苯环,故H为![]() ,由J的结构简式可知Ⅰ为
,由J的结构简式可知Ⅰ为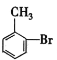 ,发生氧化反应得到J,J发生水解反应得到E,E与甲醇发生酯化反应得到F。据此解答。
,发生氧化反应得到J,J发生水解反应得到E,E与甲醇发生酯化反应得到F。据此解答。
(1)由分析可知,A的结构简式为CH2=CH2;
(2)H→I的化学方程式为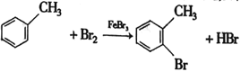 ,B与银氨溶液反应的化学方程式为CH3CHO+2Ag(NH3)2OH
,B与银氨溶液反应的化学方程式为CH3CHO+2Ag(NH3)2OH![]() CH3COONH4+2Ag↓+3NH3+H2O;
CH3COONH4+2Ag↓+3NH3+H2O;
(3)C→D是CH3COOH中—OH被—Cl取代生成CH3COCl的反应,属于取代反应;I→J是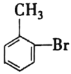 中甲基被氧化为—COOH的反应,属于氧化反应;
中甲基被氧化为—COOH的反应,属于氧化反应;
(4)两个E分子在一定条件下发生分子间脱水生成一种环状酯的结构简式是![]() ;
;
(5)①F为 ,能与FeCl3溶液发生显色反应,说明含有酚羟基;②分子中有
,能与FeCl3溶液发生显色反应,说明含有酚羟基;②分子中有![]() 结构,可能含有酯基或羧基;③苯环上有两个取代基,为—OH、—COOCH3,或—OH、—OOCCH3,或—OH、—CH2COOH,或—OH、—CH2OOCH,两个取代基均有邻、间、对三种位置关系,故符合条件的同分异构体还有11种。
结构,可能含有酯基或羧基;③苯环上有两个取代基,为—OH、—COOCH3,或—OH、—OOCCH3,或—OH、—CH2COOH,或—OH、—CH2OOCH,两个取代基均有邻、间、对三种位置关系,故符合条件的同分异构体还有11种。

【题目】甲醇既是重要的化工原料,又是电动公交车的清洁能源,利用水煤气在一定条件下合成甲醇,发生的反应为CO(g)+2H2(g)![]() CH3OH(l) ΔH=?
CH3OH(l) ΔH=?
(1)已知CO、H2、CH3OH的燃烧热分别为283.0kJ·mol-1、285.8kJ·mol-1、726.5kJ·mol-1,则ΔH=__。
(2)在一容积为2L的恒容密闭容器中加入0.2molCO和0.4molH2,发生如下反应:CO(g)+2H2(g)![]() CH3OH(g),实验测得T1℃和T2℃下,甲醇的物质的量随时间的变化如下表所示。
CH3OH(g),实验测得T1℃和T2℃下,甲醇的物质的量随时间的变化如下表所示。
时间 温度/℃ | 10min | 20min | 30min | 40min | 50min | 60min |
T1 | 0.080 | 0.120 | 0.150 | 0.168 | 0.180 | 0.180 |
T2 | 0.120 | 0.150 | 0.156 | 0.160 | 0.160 | 0.160 |
①由上述数据可以判断:T1__T2(填“>”“<”或“=”)。
②T1℃时,0~20minH2的平均反应速率v(H2)=__。
③该反应在T1℃达到平衡后,为同时提高反应速率和甲醇的生成量,以下措施一定可行的是__(填字母)。
A.改用高效催化剂
B.升高温度
C.缩小容器容积
D.分离出甲醇
E.增加CO的浓度
(3)若保持T2℃不变,起始时加入CO、H2、CH3OH的物质的量分别为amol、bmol、cmol,达到平衡时,仍与原平衡等效,则a、b、c应满足的条件:__。
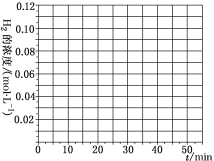
(4)当反应在T1℃进行20min时,迅速将0.02molCO、0.04molH2、0.18molCH3OH同时投入体系中,同时将反应体积扩大为原来的2倍,反应在40min时达到平衡,请在图中画出20~40min内容器中H2浓度的变化趋势曲线___。
(5)在以CH3OH(l)为燃料的燃料电池中,电解质溶液为酸性,则负极的电极反应式为__;理想状态下,该燃料电池消耗2mol甲醇所能产生的最大电能为1162.4kJ,则该燃料电池的理论效率为__(燃料电池的理论效率是指电池所产生的最大电能与燃料电池反应所能释放的全部能量之比)。