题目内容
【题目】“千年大计、国家大事”,雄安新区无疑是今年最受瞩目的地区。不过,近日媒体报道河北廊坊、天津等地存在超大规模的工业污水渗坑,给雄安新区的水环境带来隐患,目前正采用多种方法对污水进行处理,改善水资源状况。
(1)在微生物作用的条件下,废水中的NH4+经过两步反应氧化成NO3-,两步反应的能量变化示意图如下:
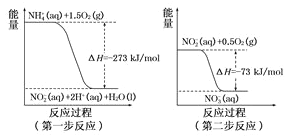
①第一步反应是______反应(选填“放热”或“吸热”),判新依据是_________。1mol NH4+ (aq)全部氧化成NO3- (aq)的热化学方程式为_____________。
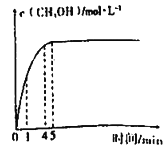
②一定条件下,向废水中加入CH3OH,将HNO3还原成N2。若该过程中CH3OH反应生成CO2,则参加反应的还原剂和氧化剂的物质的量之比为______.
(2)二氧化氯(ClO2)是一种黄绿色到橙黄色的气体,是国际上公认为安全、无毒的绿色消毒剂,可以投入废水中清除污染物。
①二氧化氯可以将废水中的氰化物(CN-)氧化成两种无污染气体.写出离子方程式________。
②废水中的重金属离子的危害性很大,二氧化氯能够在弱酸性溶液中把二价锰离子氧化成不溶于水的二氧化锰(MnO2),写出反应的离子方程式_______________。
【答案】 放热 △H=-273kJ/mol(或反应物的总能量大于生成物的总能量) NH4+(aq)+2O2(g)=2H+(aq)+NO3-(aq)+H2O(l) △H=-346kJ/mol 5:6 2ClO2+2CN-=2CO2+N2+2Cl- 2ClO2+5Mn2++6H2O=5MnO2↓+12H++2Cl-
【解析】(1)①从图中得到第一步反应的反应物的能量高于生成物的能量,所以是放热反应。从左图得到NH4+(aq)+3/2O2(g)=2H+(aq)+NO2-(aq)+H2O(l) △H=-273kJ/mol;从右图得到NO2-(aq)+1/2O2(g) = NO3-(aq) △H=-73kJ/mol;两个方程式相加得到:NH4+(aq)+2O2(g)=2H+(aq)+NO3-(aq)+H2O(l) △H=-346kJ/mol。
②明显得到氧化剂为HNO3,还原剂为CH3OH。CH3OH中的C为-2价(有机物中一般默认H为+1价,O为-2价),生成的CO2中C为+4价,所以一个CH3OH在反应中失去6个电子。HNO3中N为+5价,反应后生成的N2中N为0价,所以一个HNO3得到5个电子。为保证得失电子守恒,还原剂(CH3OH)和氧化剂(HNO3)的物质的量之比为5:6。
(2)①二氧化氯可以将废水中的氰化物(CN-)氧化成两种无污染气体,这两种无污染的气体只能是二氧化碳和氮气,二氧化氯本身被还原的产物应该是氯离子。CN-中C为+2价,N 为-3价,所以CN-要升高2+3=5价,ClO2降低5价,根据化合价升降相等和原子个数守恒配平,得到:2ClO2+2CN-=2CO2+N2+2Cl-。
②二氧化氯能够在弱酸性溶液中把二价锰离子氧化成不溶于水的二氧化锰(MnO2),本身被还原转化为氯离子,根据化合价升降相等和原子个数守恒配平,得到:2ClO2+5Mn2++6H2O=5MnO2↓+12H++2Cl-。

 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案【题目】某研究小组在实验室进行硫的化合物系列实验。
Ⅰ.验证H2SO3的酸性比H2CO3强,甲同学设计下图装置。
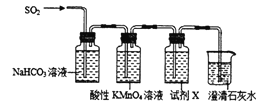
(1)试剂X的作用是_______。
(2)当观察到_______,即证明H2SO3的酸性比H2CO3强。
Ⅱ.研究铁与硫酸的反应。
已知: 浓H2SO4的沸点为338.2℃。
a.乙同学设计如下表所示的实验1、2:
实验 | 试剂 | 现象 | |
| 1 | 螺旋状铁丝、稀硫酸 | 铁丝表面有大量气体产生。 |
2 | 螺旋状铁丝、浓硫酸 | 铁丝表面迅速发黑(Fe3O4),有少量气体产生,反应很快停止。 | |
(3)上述实验中,铁丝绕成螺旋状的目的是_______。
(4)实验1中,铁与稀硫酸反应的离子方程式为_______。
(5)实险2中的现象常被称为_______。
b.丙同学设计如图所示装置的实验3:
加热试管A,温度保持在250℃~300℃,产生大量气体,B中品红褪色,D处始终未检测到可燃性气体,实验结束后,检验到A的溶液中既有Fe3+又有Fe2+。

(6)A中产生的气体是_______; 请设计实验方案检测装置A的溶液中含有Fe3+_______ (简要说明操作、试剂、现象和结论)。
(7)分析实验1、2、3,可知影响铁和硫酸反应产物多样性的因素有_______。