题目内容
【题目】2SO2(g)+O2(g)![]() 2SO3(g)反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ·mol-1。请回答下列问题:
2SO3(g)反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ·mol-1。请回答下列问题:
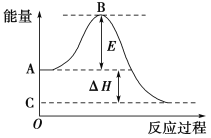
(1)图中A点表示:___________, B点表示:__________,E的大小对该反应的反应热________(填“有”或“无”)影响。
(2)图中ΔH=________kJ·mol-1。
【答案】 反应物的总能量 正反应的活化能 无 -198
【解析】(1)A、C分别表示反应物总能量的生成物总能量,B为活化能,活化能的大小与反应热无关;(2)根据参加反应SO2的物质的量之比等于对应的ΔH之比。
详解:(1)因图中A、C分别表示反应物总能量、生成物总能量,B为活化能,反应热可表示为A、C活化能的大小之差,活化能的大小与反应热无关,
因此,本题正确答案是:反应物总能量、正反应的活化能;无;
(2)因1 mol SO2氧化为1 mol SO3的ΔH=-99 kJ·mol-1,所以2mol SO2氧化为2mol SO3的ΔH=-198 kJ·mol-1,
则2SO2(g)+O2(g)![]() 2SO3(g) ΔH=-198 kJ·mol-1,因此,本题正确答案是: -198。
2SO3(g) ΔH=-198 kJ·mol-1,因此,本题正确答案是: -198。

 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案【题目】下列有关细胞物质组成的叙述,正确的是
A. 在人体活细胞中氧原子的数目最多
B. 脂肪细胞含量最多的化合物是脂肪
C. 每种细胞所含的有机物最多的都是蛋白质
D. 组成蛋白质的元素一定有C、H、O、N
【题目】某研究小组在实验室探究氨基甲酸铵(NH2COONH4)分解反应平衡常数和反应速率的测定。将一定量纯净的氨基甲酸铵固体置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)![]() 2NH3(g)+CO2(g)
2NH3(g)+CO2(g)
实验测得不同温度下的平衡数据列于下表:
温度/℃ | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
平衡气体总浓度/mol·L-1 | 2.4×10-3 | 3.4×10-3 | 4.8×10-3 | 6.8×10-3 | 9.4×10-3 |
(1)可以判断该分解反应已经达到平衡的是________。
A.2v(NH3)=v(CO2) B.密闭容器中总压强不变
C.密闭容器中混合气体的密度不变 D.密闭容器中氨气的体积分数不变
E.单位时间内消耗1 molNH2COONH4 ,同时生成2mol NH3
F.密闭容器中混合气体的平均摩尔质量不变 G.容器内NH3与CO2的浓度之比为2∶1 H.6个N—H键断裂的同时,有2个C=O键形成
(2)根据表中数据,计算25.0 ℃时的分解平衡常数______________。
(3)取一定量的氨基甲酸铵固体放在一个带活塞的密闭真空容器中,在25.0 ℃下达到分解平衡。若在恒温下压缩容器体积,氨基甲酸铵固体的质量________(填“增加”、“减少”或“不变”)