题目内容
【题目】氮、磷及其化合物在生产、生活中有重要的用途。回答下列问题:
Ⅰ.(1)氮的固定是几百年来科学家一直研究的课题。
下表列举了不同温度下大气固氮和工业固氮的部分K值。
反应 | 大气固氮 N2(g)+O2(g) | 工业固氮 N2(g)+3H2(g) | |||
温度/℃ | 27 | 2000 | 25 | 400 | 450 |
K | 3.8×10-31 | 0.1 | 5×108 | 0.507 | 0.152 |
①分析数据可知:大气固氮反应属于_____(填“吸热”或“放热”)反应。
②分析数据可知;人类不适合大规模模拟大气固氮的原因_____。
(2)NaNO2是一种食品添加剂(有毒性,市场上常误与食盐混淆)。可用酸性KMnO4溶液检验,完成其反应的离子方程式。MnO![]() +NO
+NO![]() +_____=Mn2++NO
+_____=Mn2++NO![]() +H2O。
+H2O。
(3)工业生产以NH3和CO2为原料合成尿素[CO(NH2)2],反应的化学方程式为: 2NH3(g)+CO2(g)![]() CO(NH2)2(l)+H2O(l) △H<0。T1℃时,在2 L的密闭容器中充入NH3和CO2模拟工业生产,若原料气中的NH3和CO2的物质的量之比(氨碳比)
CO(NH2)2(l)+H2O(l) △H<0。T1℃时,在2 L的密闭容器中充入NH3和CO2模拟工业生产,若原料气中的NH3和CO2的物质的量之比(氨碳比)![]() = x,如图是CO2平衡转化率(α)与氨碳比(x)的关系。
= x,如图是CO2平衡转化率(α)与氨碳比(x)的关系。
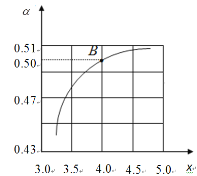
其它条件不变时,α随着x/span>增大而增大的原因是____;图中的B点处NH3的平衡转化率为____。
II.(4)红磷P(s)和Cl2 (g)发生反应生成PCl3(g)和 PCl5(g),反应过程如下。
2P(s) + 3Cl2(g)=2PCl3(g) △H1=-612 kJ· mol-1
2P(s) + 5Cl2(g)=2PCl5(g) △H2=-798 kJ· mol-1
气态PCl5生成气态PCl3和Cl2的热化学方程式为________。
(5)直链聚磷酸是由n个磷酸分子通过分子间脱水形成的,常用于制取阻燃剂聚磷酸铵。直链低聚磷酸铵的化学式可表示为(NH4)(n+2)PnOx,x=___(用n表示)。
(6)一定温度下,向浓度均为0.20 mol·L-1的MgCl2和CaCl2混合溶液中逐滴加入Na3PO4,先生成__沉淀(填化学式);当测得溶液中钙离子沉淀完全(浓度小于10-5 mol·L-1)时,溶液中的另一种金属阳离子的物质的量浓度c = ______mol·L-1。(已知:Ksp[Mg3(PO4)2] =6.0×10-29,Ksp[Ca3(PO4)2]=6.0×10-26。)
【答案】吸热 K值小,正向进行的程度小(或转化率低),不适合大规模生产; 2MnO![]() +5NO
+5NO![]() +6H+=2Mn2++5NO
+6H+=2Mn2++5NO![]() +3H2O x增大,相当于c(NH3)增大,CO2转化率增大 25% PCl5(g)
+3H2O x增大,相当于c(NH3)增大,CO2转化率增大 25% PCl5(g) ![]() PCl3(g) + Cl2(g) △H = +93 kJ·mol-1 3n+1 Mg3(PO4)2 10-6
PCl3(g) + Cl2(g) △H = +93 kJ·mol-1 3n+1 Mg3(PO4)2 10-6
【解析】
Ⅰ(1)①由表格数据可知,温度越高,K越大,说明升高温度,平衡正移,则正反应方向为吸热反应;
②由表格数据可知,2000℃时,K=0.1,K值很小,则转化率很小,不适合大规模生产,所以人类不适合大规模模拟大气固氮;
故答案为:K值小,正向进行的程度小(或转化率低),不适合大规模生产;
(2)NaNO2可用酸性KMnO4溶液检验,根据氧化还原反应相关配平原则,遵守质量守恒定律、电荷守恒定律,可以推出反应方程式为:2MnO![]() +5NO
+5NO![]() +6H+=2Mn2++5NO
+6H+=2Mn2++5NO![]() +3H2O;
+3H2O;
(3)工业以NH3和CO2为原料合成尿素[CO(NH2)2]:2NH3(g)+CO2(g)![]() CO(NH2)2(l)+H2O(l) △H<0,CO2平衡转化率(α)随(氨碳比)
CO(NH2)2(l)+H2O(l) △H<0,CO2平衡转化率(α)随(氨碳比)![]() = x的变化如图所示,氨碳比(x)越大,相当于增大
= x的变化如图所示,氨碳比(x)越大,相当于增大![]() ,故平衡正向移动,CO2平衡转化率(α)随之增大;B点对应
,故平衡正向移动,CO2平衡转化率(α)随之增大;B点对应![]() =4,且反应后CO2转化率为50%,物质的转化量之比与化学计量数呈比例关系,假设投料:
=4,且反应后CO2转化率为50%,物质的转化量之比与化学计量数呈比例关系,假设投料:![]() =4X,则
=4X,则![]() =x,又二氧化碳转化0.5x,氨气转化的是二氧化碳的2倍,故氨气转化x,氨气的转化率为:
=x,又二氧化碳转化0.5x,氨气转化的是二氧化碳的2倍,故氨气转化x,氨气的转化率为:![]() ;
;
故答案为:x增大,相当于c(NH3)增大,CO2转化率增大;25%;
II(4)根据盖斯定律及热化学方程式的书写原则,第一个反应减去第二个反应可得出气态PCl5生成气态PCl3和Cl2的热化学方程式为:2PCl5(g) ![]() 2PCl3(g)+2 Cl2(g) △H = +186 kJ·mol-1;简化后为:PCl5(g) PCl3(g) + Cl(g) △H = +93 kJ·mol-1;
2PCl3(g)+2 Cl2(g) △H = +186 kJ·mol-1;简化后为:PCl5(g) PCl3(g) + Cl(g) △H = +93 kJ·mol-1;
(5)已知直链低聚磷酸铵的化学式可表示为(NH4)(n+2)PnOx,根据化学式的书写原则,化学式的总化合价为0,铵根的化合价为+1,又氧元素为-2价,PnOx的总化合价为-(n+2)价,可以列式:![]() ,可得x=3n+1;
,可得x=3n+1;
(6)Ca3(PO4)2与Mg3(PO4)2是同类型沉淀,已知:Ksp[Mg3(PO4)2] =6.0×10-29,Ksp[Ca3(PO4)2]=6.0×10-26,故一定温度下,向浓度均为0.20 mol·L-1的MgCl2和CaCl2混合溶液中逐滴加入Na3PO4,溶度积常数小的先生成沉淀,先生成Mg3(PO4)2沉淀;当测得溶液中钙离子沉淀完全,则钙离子浓度为10-5mol·L-1,根据Ca3(PO4)2沉淀溶解平衡可知: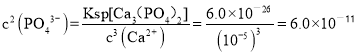 ,则在Mg3(PO4)2沉淀溶解平衡中:
,则在Mg3(PO4)2沉淀溶解平衡中: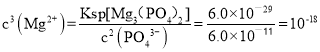 ,则
,则![]() 。
。

 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案 培优三好生系列答案
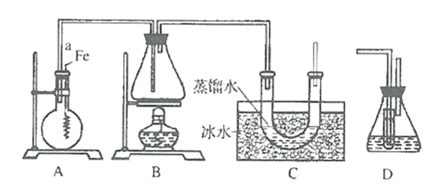
培优三好生系列答案【题目】按如图装置进行实验,下列推断正确的是( )
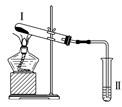
选项 | Ⅰ中试剂 | Ⅱ中试剂及现象 | 推断 |
A | 氯化铵 | 酚酞溶液不变红色 | 氯化铵稳定 |
B | 硫酸亚铁 | 品红溶液褪色 | FeSO4分解生成FeO和SO2 |
C | 涂有石蜡油的碎瓷片 | 酸性高锰酸钾溶液褪色 | 石蜡油发生了化学变化 |
D | 铁粉与水蒸气 | 肥皂水冒泡 | 铁粉与水蒸气发生了反应 |
A. A B. B C. C D. D