题目内容
【题目】轻质氧化镁和硼酸(H3BO3)都是重要的化工原料,可采用硼镁矿(含Mg2B2O5·H2O、SiO2及少量Fe2O3、Al2O3)为原料生产硼酸和轻质氧化镁,其工艺流程如图:
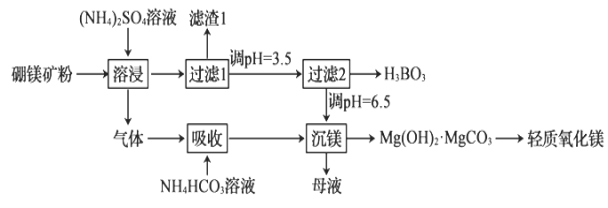
下列叙述错误的是( )
A.Fe2O3、Al2O3都不能溶于(NH4)2SO4溶液
B.进入“吸收”工序中的气体为NH3
C.若“过滤2”时调节溶液的碱性越强得到的硼酸越多
D.“沉镁”中得到的母液经加热后可返回“溶浸”工序循环使用
【答案】C
【解析】
硼镁矿含Mg2B2O5·H2O、SiO2、Fe2O3、Al2O3,加入(NH4)2SO4溶液,SiO2、Fe2O3、Al2O3不与(NH4)2SO4溶液反应,Mg2B2O5·H2O与(NH4)2SO4溶液反应,其反应方程式为:2(NH4)2SO4+ Mg2B2O5H2O +2H2O = 2MgSO4+2NH4B(OH)4+2NH3↑,NH3中加入NH4HCO4,发生反应为:NH3+ NH4HCO3= (NH4)2CO3,滤渣1为不溶于(NH4)2SO4溶液的SiO2、Fe2O3、Al2O3,滤液1调pH为3.5,将B(OH)4-转化为H3BO3,并析出H3BO3;滤液2调pH为6.5,沉镁过程中(NH4)2CO3溶液与Mg2+反应生成Mg(OH)2·MgCO3,其离子反应方程式为:2Mg2++2H2O+3CO32-= Mg(OH)2·MgCO3↓+2HCO3-。
A. SiO2、Fe2O3、Al2O3不与(NH4)2SO4溶液反应,A正确;
B. Mg2B2O5·H2O与(NH4)2SO4溶液反应,其反应方程式为:2(NH4)2SO4+ Mg2B2O5H2O +2H2O = 2MgSO4+2NH4B(OH)4+2NH3↑,即进入“吸收”工序中的气体为NH3,B正确;
C. 在“过滤2”时,将溶液pH调节至3.5,目的是得到硼酸,促进硼酸的析出,C错误;
D. 沉镁时,其离子反应方程式为:2Mg2++2H2O+3CO32-= Mg(OH)2·MgCO3↓+2HCO3-,母液的主要成分为硫酸铵,可返回“溶浸"工序中循环使用,D正确;
故答案为:C。

 优生乐园系列答案
优生乐园系列答案