题目内容
下列各组物质中,前者为强电解,后者为弱电解质的是( )
| A、氯化氢、醋酸 |
| B、硫酸、碳酸钙 |
| C、食盐、蔗糖 |
| D、碳酸、碳酸氢钠 |
考点:强电解质和弱电解质的概念
专题:电离平衡与溶液的pH专题
分析:在水溶液中完全电离的是强电解质;
在水溶液中部分电离的是弱电解质;
非电解质:在熔融状态和水溶液中都不能导电的化合物.
在水溶液中部分电离的是弱电解质;
非电解质:在熔融状态和水溶液中都不能导电的化合物.
解答:
解:A.氯化氢在水溶液中完全电离,是强电解质;醋酸在水溶液中部分电离,是弱电解质,故A正确;
B.硫酸在水溶液中完全电离,是强电解质;碳酸钙溶于水的部分完全电离,是强电解质,故B错误;
C.食盐在水溶液中完全电离,是强电解质;蔗糖在熔融状态和水溶液中都不能导电,是非电解质,故C错误;
D.碳酸在水溶液中部分电离,是弱电解质;碳酸氢钠在水溶液中完全电离,是强电解质,故D错误,
故选A.
B.硫酸在水溶液中完全电离,是强电解质;碳酸钙溶于水的部分完全电离,是强电解质,故B错误;
C.食盐在水溶液中完全电离,是强电解质;蔗糖在熔融状态和水溶液中都不能导电,是非电解质,故C错误;
D.碳酸在水溶液中部分电离,是弱电解质;碳酸氢钠在水溶液中完全电离,是强电解质,故D错误,
故选A.
点评:本题重点考查强弱电解质的判断,难度不大.要注意强电解质在水溶液中是完全电离的.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列关于钠的叙述中错误的是( )
| A、钠燃烧时发出黄色火焰,生成Na2O2 |
| B、钠投入CuSO4溶液中能生成红色的铜 |
| C、钠原子最外层有一个电子,具有强还原性 |
| D、钠与H2O反应能产生H2 |
设NA为阿佛加德罗常数的数值,下列说法正确的是( )
| A、等物质的量的H2和N2所含分子数均为NA |
| B、标准状况下,11.2L的己烷含有分子数为0.5NA |
| C、常温常压下,46g NO2含有原子数为3NA |
| D、1mol SiO2晶体中含NA个SiO2分子 |
在NH4HSO3溶液中逐滴加入Ba(OH)2溶液,下列离子方程式一定错误的是( )
| A、2HSO3-+Ba2++2OH-→BaSO3↓+SO32-+2H2O |
| B、NH4++HSO3-+Ba2++2OH-→BaSO3↓+NH3?H2O+H2O |
| C、NH4++3HSO3-+2Ba2++4OH-→2BaSO3↓+SO32-+NH3?H2O+3H2O |
| D、HSO3-+Ba2++OH-→BaSO3↓+H2O |
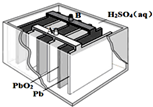 铅蓄电池是最常见的二次电池,其构造示意图如图.发生反应的化学方程式为:
铅蓄电池是最常见的二次电池,其构造示意图如图.发生反应的化学方程式为:Pb(s)+PbO2(s)+2H2SO4(aq)
| 放电 |
| 充电 |
| A、放电时,正极反应为:PbO2(s)+4H+(aq)+SO42-(aq)+2e-═PbSO4(s)+2H2O(l) |
| B、铅蓄电池广泛用于汽车启动电源,可以边使用边充电,充电时,应将充电电源的正极与铅蓄电池的接线柱A相接 |
| C、实验室用铅蓄电池做电源精炼粗铜时,应将粗铜与接线柱B相连接 |
| D、铅蓄电池做电源电解AgNO3溶液,当有标况下11.2升O2产生时,消耗2mol H2SO4 |
下列反应的离子方程式正确的是( )
| A、FeCl3溶液腐蚀铜板电路:Fe3++Cu=Fe2++Cu2+ |
| B、碳酸钙溶于醋酸溶液:CaCO3+2H+=Ca2++CO2↑+H2O |
| C、Ba(OH)2溶液与稀硫酸反应:Ba2++SO42-=BaSO4↓ |
| D、铜与稀硝酸反应:3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O |
有X,Y两种原子,对它们结构的下列描述中,能说明彼此化学性质一定相似的是( )
| A、电子排布式分别为:1s2和1s22s2 |
| B、X原子M层上只有两个电子,Y原子N层上也只有两个电子 |
| C、X原子的2p亚层上有二对成对电子,Y原子的3p亚层上也有二对成对电子 |
| D、X原子的2p亚层上只有一个未成对电子,Y原子的3p亚层上只有一个未成对电子 |
下列离子方程式中书写正确的是( )
| A、FeS固体与稀硝酸混合:FeS+2H+=2Fe2++H2S |
| B、NH4HSO4溶液中加入足量Ba(OH)2溶液:H++SO42-+Ba2++OH-═BaSO4+H2O |
| C、将少量SO2气体通入NaClO溶液中:SO2+2ClO-+H2O═SO32-+2HClO |
| D、1.12L(标况)Cl2通入1L 1mol/L的FeI2溶液中:2I-+Cl2=I2+2Cl- |
常温时,下列各溶液中有关粒子浓度的说法正确的是( )
| A、pH=5的NaHSO3溶液:c(HSO3-)>c(SO32-)>c(H2SO3) |
| B、pH=3的盐酸跟pH=11的氨水等体积混合:c(H+)>c(OH-) |
| C、pH<7的CH3COONa和CH3COOH的混合溶液 c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| D、pH=12的NaOH溶液中:c(OH-)水电离=1.0×10-12mol/L |