题目内容
【题目】我们已经学习了几种典型的有机化学反应类型,写出下列反应的化学反应方程式,并判断其反应类型。
(1)由乙醇制乙烯_____属于_____反应。
(2)由苯制取硝基苯_____属于_____反应。
(3)由乙醇制乙醛_____属于_____反应。
(4)由丙烯腈(CH2=CH-CN)制备聚丙烯腈(人造羊毛的主要成分):_____,属于_____反应。
【答案】CH3CH2OH![]() CH2=CH2↑+H2O 消去
CH2=CH2↑+H2O 消去 ![]() +HNO3(浓)
+HNO3(浓) ![]()
![]() +H2O 取代 2CH3CH2OH+O2
+H2O 取代 2CH3CH2OH+O2![]() 2CH3CHO+2H2O 氧化
2CH3CHO+2H2O 氧化 ![]() 加聚
加聚
【解析】
(1)由乙醇制乙烯,需要在乙醇分子内去掉1个-OH和1个H;
(2)由苯制取硝基苯,是将苯环上的1个氢原子用1个硝基替代;
(3)由乙醇制乙醛,是将-CH2OH转化为-CHO;
(4)由丙烯腈(CH2=CH-CN)制备聚丙烯腈,是将n个丙烯腈分子断裂碳碳双键中的1个键,然后将链节连接而成为大分子。
(1)由乙醇制乙烯,需要在浓硫酸、170℃的条件下才能实现,反应方程式为CH3CH2OH![]() CH2=CH2↑+H2O,属于消去反应。答案为:CH3CH2OH
CH2=CH2↑+H2O,属于消去反应。答案为:CH3CH2OH![]() CH2=CH2↑+H2O;消去;
CH2=CH2↑+H2O;消去;
(2)由苯制取硝基苯,需要在混酸、加热条件下才能实现,反应方程式为![]() +HNO3(浓)
+HNO3(浓) ![]()
![]() +H2O,属于取代反应。答案为:
+H2O,属于取代反应。答案为:![]() +HNO3(浓)
+HNO3(浓) ![]()
![]() +H2O;取代;
+H2O;取代;
(3)由乙醇制乙醛,需要在氧化剂的帮助下才能完成,反应的方程式为2CH3CH2OH+O2![]() 2CH3CHO+2H2O,属于氧化反应。答案为:2CH3CH2OH+O2
2CH3CHO+2H2O,属于氧化反应。答案为:2CH3CH2OH+O2![]() 2CH3CHO+2H2O;氧化;
2CH3CHO+2H2O;氧化;
(4)由丙烯腈(CH2=CH-CN)制备聚丙烯腈(人造羊毛的主要成分),需要一定条件,反应的方程式为![]()
![]()
![]() ,属于加聚反应。答案为:
,属于加聚反应。答案为:![]()
![]()
![]() ;加聚。
;加聚。

【题目】铋酸钠(NaBiO3)是分析化学中的重要试剂,在水中缓慢分解,遇沸水或酸则迅速分解。某兴趣小组设计实验制取铋酸钠并探究其应用。回答下列问题:
Ⅰ.制取铋酸钠
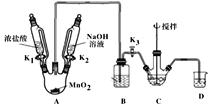
制取装置如图(加热和夹持仪器已略去),部分物质性质如下:
物质 | NaBiO3 | Bi(OH)3 |
性质 | 不溶于冷水,浅黄色 | 难溶于水;白色 |
(1)B装置用于除去HCl,盛放的试剂是___;
(2)C中盛放Bi(OH)3与NaOH混合物,与Cl2反应生成NaBiO3,反应的离子方程式为___;
(3)当观察到___(填现象)时,可以初步判断C中反应已经完成;
(4)拆除装置前必须先除去烧瓶中残留Cl2以免污染空气。除去Cl2的操作是___;
(5)反应结束后,为从装置C中获得尽可能多的产品,需要的操作有___;
Ⅱ.铋酸钠的应用——检验Mn2+
(6)往待测液中加入铋酸钠晶体,加硫酸酸化,溶液变为紫红色,证明待测液中存在Mn2+。
①产生紫红色现象的离子方程式为___;
②某同学在较浓的MnSO4溶液中加入铋酸钠晶体,加硫酸酸化,结果没有紫红色出现,但观察到黑色固体(MnO2)生成。产生此现象的离子反应方程式为___。
Ⅲ.产品纯度的测定
(7)取上述NaBiO3产品wg,加入足量稀硫酸和MnSO4稀溶液使其完全反应,再用cmo1·L-1的H2C2O4标准溶液滴定生成的MnO4-(已知:H2C2O4+MnO4-——CO2+Mn2++H2O,未配平),当溶液紫红色恰好褪去时,消耗vmL标准溶液。
该产品的纯度为___(用含w、c、v的代数式表示)。