题目内容
【题目】利用含碳化合物合成燃料是解决能源危机的重要方法,已知煤液化过程中有反应CO(g)+2H2(g)=CH3OH(g),其反应过程中的能量变化情况如图所示,曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。下列判断正确的是( )
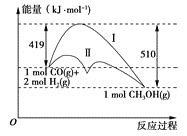
A.该反应的反应热ΔH=+91kJ·mol-1
B.加入催化剂后,该反应的ΔH变小
C.反应物的总能量大于生成物的总能量
D.从图中可以看出,使用催化剂降低了该反应的活化能
【答案】CD
【解析】
A. 该反应的反应热ΔH= 419kJmol1510 kJmol1=91 kJmol1,故A错误;
B. 催化剂可改变反应速率,但不改变反应热,故B错误;
C. 该反应为放热反应,反应物的总能量高于生成物的总能量,故C正确;
D. 使用催化剂可降低反应所需的活化能,故D正确。
综上所述,答案为CD。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目