��Ŀ����
6����ӦmA+nB?pC��ij�¶��´ﵽƽ�⣮��1����A��B��C�������壬��ѹ������Ӧ����С���淴Ӧ���ʣ���m��n��p�Ĺ�ϵ��m+n��p��
��2��������ϵ�����ӻ����B������ƽ����������ƶ�����B�϶�����Ϊ��̬��
��3����AΪҺ�壬CΪ���壬��m+n=p���ڼ�ѹʱ��ѧƽ�ⷢ���ƶ�����ƽ��ض����淴Ӧ�������Ӧ�����淴Ӧ���������ƶ���
��4���������¶ȣ�A���ʵ�ת����������÷�ӦΪ���ȣ�����ȡ����ȡ�����Ӧ��
���� ��1������Ӱ�컯ѧƽ�����ؽ�����ʴ�С�����жϷ�Ӧǰ�������仯��
��2����Ӧǰ��ϵ����ͬ���ı�ѹǿƽ���ƶ�˵����Ӧ���к��й����Һ�壻
��3������ʹ�Һ���ƽ����Ӱ�죻
��4���������¶ȣ�A���ʵ�ת��������˵��ƽ��������У�����ƽ���ƶ�ԭ��������ӦΪ���ȷ�Ӧ��
��� �⣺��1����ӦmA+nB?pC����A��B��C�������壬��ѹ������Ӧ����С���淴Ӧ���ʣ�֤������Ӧ�������������ķ�Ӧ���õ�m+n��p��
�ʴ�Ϊ��m+n��p��
��2������ӦmA+nB?pC���������ϵ�����ӻ����B������ƽ����������ƶ���֤��Bһ���ǹ����Һ�壬�������壬
�ʴ�Ϊ������
��3������ӦmA+nB?pC��CΪ���壬��m+n=p���ڼ�ѹʱ��ѧƽ�ⷢ���ƶ���˵��AB��������һ���ǹ����Һ�壬��ѹƽ��������У�
�ʴ�Ϊ���淴Ӧ��
��4���������¶ȣ�A���ʵ�ת��������˵��ƽ��������У�����ƽ���ƶ�ԭ������������ӦΪ���ȷ�Ӧ��
�ʴ�Ϊ�����ȣ�
���� ���⿼���˻�ѧƽ���Ӱ�������жϣ���Ҫ����ѹǿ��ƽ���Ӱ����������ʵ��жϣ���ѧƽ����ƶ������ǽ���Ĺؼ�����Ŀ�ϼ�

��ϰ��ϵ�д�
�����Ŀ
17����NAΪ����٤��������ֵ������˵����ȷ���ǣ�������
| A�� | 1L1mol•L-1��Na2CO3��Һ�к���CO32-����ĿΪNA | |
| B�� | 28g����ϩ�ͱ�ϩ�к�̼ԭ����ĿΪNA | |
| C�� | ��״���£�6.72LNO2��ˮ��ַ�Ӧת�Ƶĵ�����ĿΪ0.1NA | |
| D�� | ���³�ѹ�£�14g��N2��CO��ɻ�����庬�е�ԭ����ĿΪNA |
17�� ������̼���������ЧӦ����Ҫ���壬������̼�Ļ����������Ǽ�������ЧӦ����Ч;��֮һ��
������̼���������ЧӦ����Ҫ���壬������̼�Ļ����������Ǽ�������ЧӦ����Ч;��֮һ��
��1��������̼������������ȡ���飮��֪��
CH4��g��+CO2��g��?2CO��g��+2H2��g����H1=+247kJ•mol-1
CH4��g��+H2O��g��?CO��g��+3H2��g����H2=+205kJ•mol-1
��ӦCO2��g��+4H2��g��?CH4��g��+2H2��g���ġ�H3-163kJ/mol��
��2��һ��ѹǿ�£���ij�����ܱ������У�����H2��CO2������Ӧ��2CO2��g��+6H2��g��?CH3CH2OH��g��+3H2O��g��������ʼͶ�ϱȡ��¶���CO2��ת���ʵĹ�ϵ��ͼ��ʾ��
�ٽ����¶ȣ�ƽ��������Ӧ�����ƶ���
����700K����ʼͶ�ϱ�$\frac{n��{H}_{2}��}{n��C{O}_{2}��}$=1.5ʱ��H2��ת����Ϊ40%�����ﵽƽ���H2��Ũ��Ϊamol•L-1����ﵽƽ��ʱCH2CH2OH��Ũ��Ϊ$\frac{a}{9}$mol/L��
��3��CO2��H2��һ�������¿ɺϳɶ����ѣ�2CO2��g��+6H2��g��?CH3OCH3��g��+2H2O��g����H����һ��ѹǿ�£���2.5molH2��amolCO2�����ݻ�Ϊ1L���ܱ������У�����������Ӧ���ﵽƽ��״̬ʱ����÷�Ӧ��ʵ���������±���
��x��y�Ĵ�С��ϵΪB��
A��x=y B��x��y C��x��y D�����ж�
�����й��ڸ÷�Ӧ��������ȷ����ABC��
A���÷�Ӧ�ġ�H��0����S��0 B���÷�Ӧ��ƽ�ⳣ�����¶����߶���С
C��ת���ʷֱ�Ϊz��wʱ���ﵽƽ���ʱ��ǰ�߳� D��ת���ʷֱ�Ϊy��wʱ��ƽ�ⳣ����ͬ��
 ������̼���������ЧӦ����Ҫ���壬������̼�Ļ����������Ǽ�������ЧӦ����Ч;��֮һ��
������̼���������ЧӦ����Ҫ���壬������̼�Ļ����������Ǽ�������ЧӦ����Ч;��֮һ����1��������̼������������ȡ���飮��֪��
CH4��g��+CO2��g��?2CO��g��+2H2��g����H1=+247kJ•mol-1
CH4��g��+H2O��g��?CO��g��+3H2��g����H2=+205kJ•mol-1
��ӦCO2��g��+4H2��g��?CH4��g��+2H2��g���ġ�H3-163kJ/mol��
��2��һ��ѹǿ�£���ij�����ܱ������У�����H2��CO2������Ӧ��2CO2��g��+6H2��g��?CH3CH2OH��g��+3H2O��g��������ʼͶ�ϱȡ��¶���CO2��ת���ʵĹ�ϵ��ͼ��ʾ��
�ٽ����¶ȣ�ƽ��������Ӧ�����ƶ���
����700K����ʼͶ�ϱ�$\frac{n��{H}_{2}��}{n��C{O}_{2}��}$=1.5ʱ��H2��ת����Ϊ40%�����ﵽƽ���H2��Ũ��Ϊamol•L-1����ﵽƽ��ʱCH2CH2OH��Ũ��Ϊ$\frac{a}{9}$mol/L��
��3��CO2��H2��һ�������¿ɺϳɶ����ѣ�2CO2��g��+6H2��g��?CH3OCH3��g��+2H2O��g����H����һ��ѹǿ�£���2.5molH2��amolCO2�����ݻ�Ϊ1L���ܱ������У�����������Ӧ���ﵽƽ��״̬ʱ����÷�Ӧ��ʵ���������±���
| �¶�/K CO2ת����/% a/mol | 500 | 600 | 700 | 800 |
| 1.67 | x | 33 | ||
| 1.25 | 60 | 43 | y | |
| 0.83 | z | 32 | w |
A��x=y B��x��y C��x��y D�����ж�
�����й��ڸ÷�Ӧ��������ȷ����ABC��
A���÷�Ӧ�ġ�H��0����S��0 B���÷�Ӧ��ƽ�ⳣ�����¶����߶���С
C��ת���ʷֱ�Ϊz��wʱ���ﵽƽ���ʱ��ǰ�߳� D��ת���ʷֱ�Ϊy��wʱ��ƽ�ⳣ����ͬ��
18�� �¶�ΪTʱ����2.0L�����ܱ������г���1.0mol PCl5����ӦPCl5��g��?PCl3��g��+Cl2��g������һ��ʱ���ﵽƽ�⣮��Ӧ�����вⶨ��n��PCl3����ʱ��ı仯��ͼ������˵����ȷ���ǣ�������
�¶�ΪTʱ����2.0L�����ܱ������г���1.0mol PCl5����ӦPCl5��g��?PCl3��g��+Cl2��g������һ��ʱ���ﵽƽ�⣮��Ӧ�����вⶨ��n��PCl3����ʱ��ı仯��ͼ������˵����ȷ���ǣ�������
 �¶�ΪTʱ����2.0L�����ܱ������г���1.0mol PCl5����ӦPCl5��g��?PCl3��g��+Cl2��g������һ��ʱ���ﵽƽ�⣮��Ӧ�����вⶨ��n��PCl3����ʱ��ı仯��ͼ������˵����ȷ���ǣ�������
�¶�ΪTʱ����2.0L�����ܱ������г���1.0mol PCl5����ӦPCl5��g��?PCl3��g��+Cl2��g������һ��ʱ���ﵽƽ�⣮��Ӧ�����вⶨ��n��PCl3����ʱ��ı仯��ͼ������˵����ȷ���ǣ�������| A�� | ��Ӧ��ǰ50s��ƽ������v��PCl5��=0.0032 mol•L-1•s-1 | |
| B�� | �÷�Ӧ��ƽ�ⳣ��K=0.025 | |
| C�� | ��ͬ�¶��£���ʼʱ�������г���1.0molPCl5��0.20molPCl3 ��0.20mol Cl2����Ӧ�ﵽƽ��ǰv��������v���棩 | |
| D�� | ���������������䣬�����¶ȣ�ƽ��ʱ��c��PCl3��=0.11mol•L-1����Ӧ�ġ�H��0 |
15��3.6gij���ʺ��еķ�����ĿΪ1.204��10 23��������ʵ�Ħ������Ϊ��������
| A�� | 18 g | B�� | 18 g��•mol-1 | C�� | 36 g | D�� | 36 g•mol-l |

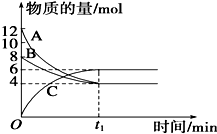 ij�¶�ʱ����VL�ܱ������У�A��B��C�������ʵ����ʵ�����ʱ��仯��������ͼ��ʾ����ͼ�����ݷ�����
ij�¶�ʱ����VL�ܱ������У�A��B��C�������ʵ����ʵ�����ʱ��仯��������ͼ��ʾ����ͼ�����ݷ����� ��ѧ������̫���ֽܷ�ˮ���ɵ������ڴ����������������̼��Ӧ���ɼ״�����������ֱ���Լ״�Ϊȼ�ϵ�ȼ�ϵ�أ���֪H2��g����CO��g����CH3OH��l����ȼ���ȡ�H�ֱ�Ϊ-285.8kJ•mol-1��-283.0kJ•mol-1��-726.5kJ•mol-1����ش��������⣺
��ѧ������̫���ֽܷ�ˮ���ɵ������ڴ����������������̼��Ӧ���ɼ״�����������ֱ���Լ״�Ϊȼ�ϵ�ȼ�ϵ�أ���֪H2��g����CO��g����CH3OH��l����ȼ���ȡ�H�ֱ�Ϊ-285.8kJ•mol-1��-283.0kJ•mol-1��-726.5kJ•mol-1����ش��������⣺