题目内容
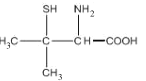
【题目】Wilson病是一种先天性铜代谢障碍性疾病,D-青霉胺具有排铜作用,用以治疗或控制Wilson病症。D-青霉胺结构简式如图:
回答下列问题:
(1)写出Cu的简化电子排布式________。
(2)已知气态基态原子得到一个电子形成气态基态负一价离子所产生的能量变化称为该元素原子的第一电子亲合能(吸收能量为负值,释放能量为正值),试解释碳原子第一电子亲合能较大的原因 _________。 第一电子亲合能可能为正值或负值,而第二电子亲合能均为负值,原因是_____。
(3)D-青霉胺中,硫原子的VSEPR模型为____,碳原子的杂化方式为_______。
(4)请简述D-青霉胺能溶于水的主要原因________。
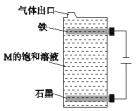
(5)青霉胺在临床治疗时对于症状改善较慢,常有并发症出现,因而近年采用锌剂(ZnSO4)替代治疗,可由硫化锌制备。立方硫化锌晶胞与金刚石晶胞类似,结构如图
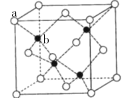
其中a代表S2-,b代表Zn2+。则该晶胞中S2-的配位数为______,若晶体的密度为ρg·cm-3,则晶胞的体积为________ cm3(列出计算式)。
【答案】[Ar]3d104s1 碳原子 2p 能级有两个电子,得到一个电子后 2p 能级为半充满,能量低更稳定 原子得到一个电子后显负电性,若要再得电子会有较大的排斥力,需要吸收能量 四面体形 sp2、sp3 D-青霉胺中的羧基、氨基能与水分子间形成氢键 4 (65+32)×4/ρNA
【解析】
(1)Cu为29号元素,其简化电子排布式为[Ar]3d104s1;
(2)碳原子 2p 能级有两个电子,得到一个电子后 2p 能级为半充满,能量低更稳定,所以碳原子第一电子亲合能较大;原子得到一个电子后显负电性,若要再得电子会有较大的排斥力,需要吸收能量,所以第二电子亲合能为负值;
(3)根据D-青霉胺的结构简式可知S原子与氢原子形成一个σ键,与碳原子形成一个σ键,同时还有两对孤电子对,所以为sp3杂化,VSEPR模型为四面体形;形成羧基的碳原子与氧原子形成一个碳氧双键,为sp2杂化,其他碳原子均为饱和碳原子,均为sp3杂化;
(4)D-青霉胺中的羧基、氨基均为亲水基,能与水分子间形成氢键;
(5)已面心的S2-为研究对象,每个晶胞内部有2个距离S2-相等且最近的Zn2+,所以该晶胞中S2-的配位数为4;根据均摊法,该晶胞含有S2-个数为![]() =4,含有Zn2+的个数为4,所以晶胞的质量m=
=4,含有Zn2+的个数为4,所以晶胞的质量m=![]() ,所以晶胞的体积V=
,所以晶胞的体积V=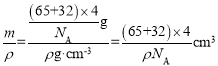 。
。

 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案