题目内容
【题目】高氯酸铵是一种常见的强氧化剂,常用作火箭发射的推进剂。根据下列信息回答问题:
已知:①高氯酸铵受热分解为N2、Cl2、O2和H2O;②Mg3N2易水解;③Cu与N2在酒精灯加热条件下不反应。
(1)写出高氯酸铵受热分解的化学反应方程式: _____________,Mg3N2的电子式为________。
(2)现有23.5g NH4ClO4分解,用下列装置设计实验,验证其分解产物并计算分解率。(注:①装置中空气已除尽;②装置可重复使用;③B~F装置中的试剂均过量且能与相应物质反应完全。)
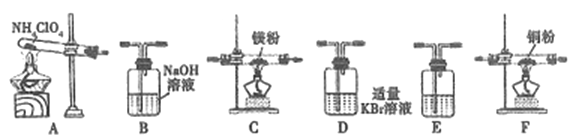
①用E装置质量的增加来验证生成的气体产物之一,则E中盛放的试剂是:_______。
②请按气流由左至右的方向连接装置:A →E→D →B→______→_____→_______→E (选择B~F装置,并用B~F字母填空)。
③证明产物中有Cl2的实验现象:________。
④反应结束后,若C装置质量增加了2.38g,则NH4ClO4的分解率是:________%。
(3)样品中NH4ClO4的含量(杂质中不含NH4+)还可用蒸馏法测定(如图所示,加热和夹持装置已略去),实验步骤如下:

步骤1:组装仪器,检查气密性;准确称取样品a g(不超过0.5g)于蒸馏烧瓶中,加入约150mL水溶解。
步骤2:准确量取40.00mL 约0.1mol/L H2SO4于锥形瓶中。
步骤3:向蒸馏烧瓶中加入20mL 3mol/L NaOH溶液;加热蒸馏使NH3全部挥发。
步骤4:用新煮沸过的水冲洗冷凝装置2~3次,洗涤液并入锥形瓶中。
步骤5:向锥形瓶中加2~3滴甲基橙,用c mol/L NaOH标准溶液滴定至终点,消耗NaOH标准溶液V1 mL。
步骤6:重复实验2~3次。
回答下列问题:
①步骤2中,准确量取40.00ml H2SO4 溶液的玻璃仪器是: __________。
②为获得样品中NH4ClO4的含量,还需补充的实验是:______。
【答案】2NH4ClO4![]() 2O2↑+N2↑+Cl2↑+4H2O↑
2O2↑+N2↑+Cl2↑+4H2O↑ ![]() 浓硫酸 E、F、C D裝置中颜色由无色变为橙色 85.0或85 酸式滴定管或移液管 用NaOH标准溶液标定硫酸溶液的浓度
浓硫酸 E、F、C D裝置中颜色由无色变为橙色 85.0或85 酸式滴定管或移液管 用NaOH标准溶液标定硫酸溶液的浓度
【解析】
试题(1)根据得失电子守恒配平高氯酸铵受热分解的化学反应方程式;Mg3N2是离子化合物;(2)A是高氯酸铵受热分解的装置;B是氢氧化钠溶液,可以吸收氯气;C中盛放Mg粉,可以检验氮气;D中溴化钾可以检验氯气;F中铜粉可以检验氧气;E中盛放液体,根据E装置质量的增加来验证生成的水,所以E中盛浓硫酸;(3) ①根据硫酸体积的精度是0.01mL选择仪器;②要计算NH4ClO4的含量,需要知道硫酸溶液的浓度。
解析:(1)根据得失电子守恒配平高氯酸铵受热分解的化学反应方程式为2NH4ClO4![]() 2O2↑+N2↑+Cl2↑+4H2O↑;Mg3N2是离子化合物,电子式是
2O2↑+N2↑+Cl2↑+4H2O↑;Mg3N2是离子化合物,电子式是![]() ;(2)①A是高氯酸铵受热分解的装置;B是氢氧化钠溶液,可以吸收氯气;C中盛放Mg粉,可以检验氮气;D中溴化钾可以检验氯气;F中铜粉可以检验氧气;E中盛放液体,根据E装置质量的增加来验证生成的水,所以E中盛浓硫酸;②根据以上分析,按气流由左至右的方向连接装置:A →E→D →B→E→F→C→E;③D中溴化钾可以与氯气反应,方程式是
;(2)①A是高氯酸铵受热分解的装置;B是氢氧化钠溶液,可以吸收氯气;C中盛放Mg粉,可以检验氮气;D中溴化钾可以检验氯气;F中铜粉可以检验氧气;E中盛放液体,根据E装置质量的增加来验证生成的水,所以E中盛浓硫酸;②根据以上分析,按气流由左至右的方向连接装置:A →E→D →B→E→F→C→E;③D中溴化钾可以与氯气反应,方程式是![]() ,溴水为橙色,所以D裝置中颜色由无色变为橙色可以证明产物中有Cl2;④C中盛放Mg粉,可以与氮气反应生成Mg3N2,若C装置质量增加了2.38g,说明反应生成氮气2.38g,则NH4ClO4的分解率是
,溴水为橙色,所以D裝置中颜色由无色变为橙色可以证明产物中有Cl2;④C中盛放Mg粉,可以与氮气反应生成Mg3N2,若C装置质量增加了2.38g,说明反应生成氮气2.38g,则NH4ClO4的分解率是![]() ;(3) ①根据硫酸体积的精度是0.01mL,准确量取40.00ml H2SO4 溶液的玻璃仪器是酸式滴定管;②为获得样品中NH4ClO4的含量,还需补充的实验是用NaOH标准溶液标定硫酸溶液的浓度。
;(3) ①根据硫酸体积的精度是0.01mL,准确量取40.00ml H2SO4 溶液的玻璃仪器是酸式滴定管;②为获得样品中NH4ClO4的含量,还需补充的实验是用NaOH标准溶液标定硫酸溶液的浓度。

【题目】工业上以硫酸泥(主要含S、Se、Fe2O3、CuO、ZnO、SiO2等)为原料提取硒,流程如图:

(1)“脱硫”过程中,温度控制在95℃,原因是___。
(2)“氧化”过程中,Se转化成H2SeO3,该反应的化学方程式为___。
(3)“还原”过程是通过控制电位还原的方法将电位高的物质先还原,电位低的物质保留在溶液中。下表是将“过滤Ⅰ”所得滤液中所含物质还原对应的电位。控制电位在0.782~1.692V,可除去“过滤Ⅰ”所得滤液中残留的ClO2。
名称 | Cu2+/Cu | Zn2+/Zn | Fe2+/Fe | Fe3+/Fe2+ | ClO2/Cl- | H2SeO3/Se |
电位/V | 0.435 | -0.885 | -0.463 | 0.782 | 1.692 | 0.743 |
为使硒和杂质金属分离,加入Na2SO3还原时,电位应控制在___范围;H2SeO3(弱酸)还原为硒的离子反应方程式为___。
(4)滤液Ⅱ中主要存在的金属阳离子有Zn2+、Na+、___。
(5)所得粗硒需精制。向粗硒浸出液中加入Na2S溶液可以将残留的Fe2+等微量杂质离子转化为沉淀而除去。已知25℃时Ksp(FeS)=6.0×10-18,要使溶液中Fe2+沉淀完全[c(Fe2+)≤1.0×10-5mol·L-1],则需控制溶液中c(S2-)≥___mol·L-1。