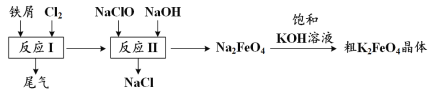题目内容
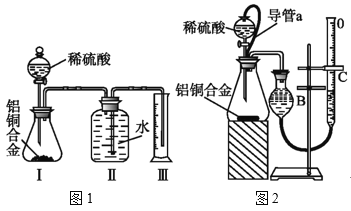
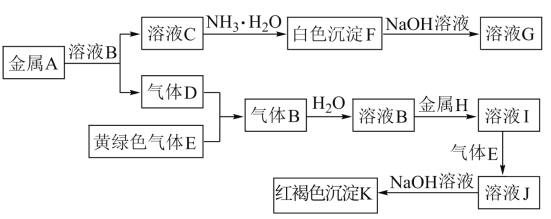
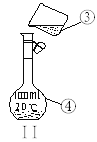
【题目】下列实验现象预测正确的是
A | B | C | D |
|
|
|
|
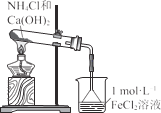
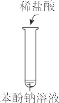
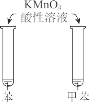
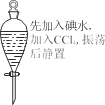
烧杯中产生白色沉淀,一段时间后沉淀无明显变化 | 加盐酸出现白色浑浊,加热变澄清 | KMnO4 酸性溶液在苯和甲苯中均褪色 | 液体分层,下层呈 无色 |
A.AB.BC.CD.D
【答案】B
【解析】
A.氯化铵和氢氧化钙固体受热分解生成氨气,氨气与氯化亚铁溶液反应,立即生成白色沉淀,白色沉淀迅速变为灰绿色,最终变为红褐色,故A错误;
B.苯酚钠溶液与盐酸反应生成苯酚,出现白色浑浊,由于苯酚溶于热水,则加热变澄清,故B正确;
C.苯不能与酸性高锰酸钾溶液反应,不能使酸性高锰酸钾溶液褪色,故C错误;
D.四氯化碳比水的密度大,碘在四氯化碳中溶解度大于水中溶解度,则分层后,下层碘的四氯化碳溶液呈紫色或紫红色,故D错误;
故选B。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目