题目内容
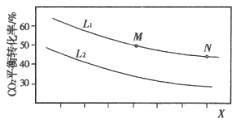
【题目】合成乙烯的主要反应:6H2(g)+2CO2(g)![]() CH2=CH2(g)+4H2O(g) △H<0。图中L(L1、L2)、Ⅹ可分别代表压强或温度。下列说法正确的是
CH2=CH2(g)+4H2O(g) △H<0。图中L(L1、L2)、Ⅹ可分别代表压强或温度。下列说法正确的是
A. L1<L2
B. X代表压强
C. M、N两点对应的平衡常数相同
D. M点的正反应速率v正小于N点的逆反应速率v逆
【答案】D
【解析】
合成乙烯的主要反应: 6H2 (g)+2CO2 (g) ![]() CH2=CH2 (g) +4H2O (g) △H<0,由图知X越大二氧化碳的平衡转化率减小,说明平衡逆向移动,所以X是温度的变化,而L1和L2为等压线,由此分析解答。
CH2=CH2 (g) +4H2O (g) △H<0,由图知X越大二氧化碳的平衡转化率减小,说明平衡逆向移动,所以X是温度的变化,而L1和L2为等压线,由此分析解答。
A. L1 对应二氧化碳的转化率高,所以L1>L2,选项A错误;
B. X代表温度,选项B错误;
C. M、N对应温度不同,所以两点对应的平衡常数不相同,选项C错误;
D.温度越高反应速率越快,所以M点的正反应速率V正小于N点的逆反应速率V逆,选项D正确;
答案选D。

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案
相关题目
【题目】如图①、②、③、④、⑤五组仪器(可重复使用),选择合适的装置和药品能完成的实验是( )

选项 | 实验目的 | 实验装置 | 实验药品 |
A | 制备并收集HCl气体 | ①③④ | 浓盐酸、浓硫酸、水 |
B | 比较氯气和溴的氧化性强弱 | ①③③⑤ | MnO2、浓盐酸、饱和食盐水、溴化钾溶液、氢氧化钠溶液 |
C | 探究乙烯的加成反应 | ①③ | 无水乙醇、浓硫酸、溴的四氯化碳溶液 |
D | 探究二氧化硫的还原性 | ②③③ | 亚硫酸钠、30%的硝酸、溴水、氢氧化钠溶液 |
A. AB. BC. CD. D