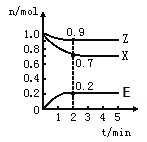
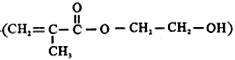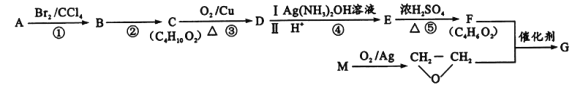题目内容
【题目】一定条件下,在某恒容密闭容器中进行反应X(g) + 3Y(g)![]() 2Z(g),若X、Y、Z起始浓度分别为c1 mol/L、c2 mol/L、c3 mol/L(c1、c2、c3均大于0),当反应达平衡时X、Y、Z的浓度分别为0.1mol/L,0.3mol/L,0.08mol/L,则下列判断不合理的是
2Z(g),若X、Y、Z起始浓度分别为c1 mol/L、c2 mol/L、c3 mol/L(c1、c2、c3均大于0),当反应达平衡时X、Y、Z的浓度分别为0.1mol/L,0.3mol/L,0.08mol/L,则下列判断不合理的是
A. c1:c2 = 1:3
B. 当4v(X)正= v(Y)逆时,该反应还在向正反应方向建立平衡
C. c1可能为0.1
D. X、Y的转化率相等
【答案】B
【解析】在化学反应中,若反应物的起始投料的物质的量之比等于它们的化学计量数之比,由于反应过程中变化量之比等于化学计量数之比,所以反应物的平衡量之比必然也等于化学计量数之比,各种反应物的转化率一定相等。由题中信息可知,当反应达平衡时X、Y的浓度分别为0.1mol/L、0.3mol/L,X、Y的平衡量之比等于化学计量数之比,所以其起始量之比一定也等于1:3, A和D正确;因为有起始投料与平衡量相同的可能,所以C正确;当4v(X)正= v(Y)逆时,因为3v(X)正= v(Y)正,所以v(Y)逆> v(Y)正,该反应还在向逆反应方向建立平衡,B不正确,选B。

练习册系列答案
 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案
相关题目