题目内容
【题目】利用右图装置,完成很多电化学实验。下列有关此装置的叙述中,不正确的是
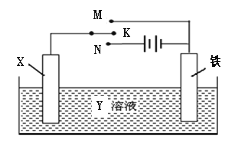
A.若X为锌棒,Y为NaCl溶液,开关K置于M处,可减缓铁的腐蚀,这种方法称为牺牲阳极的阴极保护法
B.若X为碳棒,Y为NaCl溶液,开关K置于N处,可减缓铁的腐蚀,溶液中的阳离子向铁电极移动
C.若X为铜棒,Y为硫酸铜溶液,开关K置于M处,铜棒质量将增加,此时外电路中的电子向铜电极移动
D.若X为铜棒,Y为硫酸铜溶液,开关K置于N处,铁棒质量将增加,溶液中铜离子浓度将减小
【答案】D
【解析】
试题分析:A.开关K置于M处,构成原电池,此时锌是负极,铁是正极,被保护,属于牺牲阳极的阴极保护法,故A正确;B.若X为碳棒,Y为NaCl溶液,开关K置于N处,则相当于电解氯化钠溶液,铁是阴极被保护,溶液中的阳离子向阴极移动,故B正确;C.若开关K置于M处,则构成原电池,铁比铜活泼,铁作负极,铜作正极,溶液中的铜离子在阴极放电,电子经导线传递到正极铜上,故C正确;D.若开关K置于N处,则构成电解池,铜和电源的正极相连,作阳极,失去电子,被氧化发生氧化反应。铁是阴极,溶液中的铜离子在阴极放电,相当于在铁上镀铜,溶液中的铜离子浓度几乎是不变的,故D错误。故选D。

练习册系列答案
相关题目