题目内容
【题目】硫酸铵是化工、染织、医药、皮革等工业原料。某硫酸工厂利用副产品Y处理尾气SO2得到CaSO4,再与相邻的合成氨工厂联合制备(NH4)2SO4,工艺流程如下:
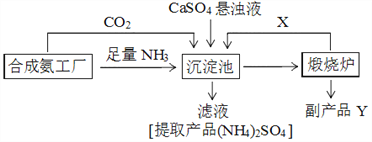
请回答以下问题:
(1)下列有关(NH4)2SO4溶液的说法正确的是_____
A.电离方程式:(NH4)2SO4![]() 2NH4++SO42-
2NH4++SO42-
B.水解离子方程式:NH4++H2O![]() NH3H2O+H+
NH3H2O+H+
C.离子浓度关系:c(NH4+)+c(H+)=c(SO42-)+c(OH–)
D.微粒浓度大小:c(NH4+)>c(SO42-)>c(H+)>c(NH3H2O)>c(OH–)
(2)硫酸工业中,V2O5作催化剂时发生反应2SO2+ O2 ![]() 2SO3,SO2的转化率与温度、压强有关,请根据下表信息,结合工业生产实际,选择下表中最合适的温度和压强分别是__________。该反应420℃时的平衡常数_____520℃时的平衡常数(填“>”、“<”或“=”)。
2SO3,SO2的转化率与温度、压强有关,请根据下表信息,结合工业生产实际,选择下表中最合适的温度和压强分别是__________。该反应420℃时的平衡常数_____520℃时的平衡常数(填“>”、“<”或“=”)。
| 1.01×105Pa | 5.05×105Pa | 1.01×106Pa |
420℃ | 0.9961 | 0.9972 | 0.9984 |
520℃ | 0.9675 | 0.9767 | 0.9852 |
620℃ | 0.8520 | 0.8897 | 0.9276 |
(3)在2L密闭容器中模拟接触法制备三氧化硫时,若第12分钟恰好达到平衡,测得生成SO3的物质的量为1.2mol,计算前12分钟用氧气表示反应速率v(O2)为___________。
(4)副产品Y是__。沉淀池中发生的主要反应方程式是___________________。
(5)从绿色化学和资源综合利用的角度说明上述流程的主要优点是________________。
【答案】 BD 420℃、1.01×105Pa > 0.025mol/(L.min) 氧化钙 CaSO4+CO2+2NH3+H2O==CaCO3↓+(NH4)2SO4 产生的CO2循环使用,物质充分利用,副产品有用,无污染性物质产生
【解析】本题分析:本题主要考查对于“工业制备(NH4)2SO4的工艺流程”的评价,涉及硫酸铵的水解等。
(1)A.(NH4)2SO4是强电解质,要用等号表示电离方程式,故A错误;B.正确;C.SO42-带2个单位负电荷,离子的电荷浓度关系:c(NH4+)+ c(H+ ) = 2c(SO42- ) +c(OH–),故C错误; D. NH4+的水解程度小,从(NH4)2SO4的组成可以看出:c(NH4+) >c(SO42-)。溶液中的变化:H2O![]() H++OH-,
H++OH-,![]() +H2O
+H2O![]() NH3 ·H2O+H+,所以 c(H+) > c(NH3H2O )>c(OH–) 。总之,c(NH4+) >c(SO42-) > c(H+) > c(NH3H2O )>c(OH–),故D正确。故选BD。
NH3 ·H2O+H+,所以 c(H+) > c(NH3H2O )>c(OH–) 。总之,c(NH4+) >c(SO42-) > c(H+) > c(NH3H2O )>c(OH–),故D正确。故选BD。
(2)在420℃、1.01×105Pa时,转化率已相当高,没有必要加压,所以最合适的温度和压强分别是420℃、1.01×105Pa。该反应升温平衡左移,所以420℃时的平衡常数大于520℃时的平衡常数。
(3)v(SO3)=(1.2/12/2) mol/(L.min)= 0.05mol/(L.min), v(O2)= v(SO3)/2=0.025mol/(L.min)。
(4)副产品Y是氧化钙。沉淀池中发生的主要反应的化学方程式是CaSO4+CO2+2NH3+H2O=CaCO3↓+(NH4)2SO4。
(5)从绿色化学和资源综合利用的角度,上述流程的主要优点是产生的CO2循环使用,物质充分利用,副产品有用,无污染性物质产生。