��Ŀ����
����Ŀ������Ҫ0.2 mol��L1CuSO4��Һ250 mL��ʵ���ҳ�����ˮ��ṩ��ɫ��������(CuSO4��5H2O)��4 mol��L1CuSO4��Һ�����Լ������Ƹ���Һ��
(1)���۲��ú����Լ��������ƣ����ձ�������������ͷ�ι��⣬���ٻ������õ���һ�ֲ���������___________����ʹ�ø�����ǰ������еIJ�����______________________��
(2)���õ�������������ƣ�����������ƽ��ȡCuSO4��5H2O������Ϊ___________ g�������4 mol/L��CuSO4��Һϡ�����ƣ�������Ͳ��ȡ___________mL 4 mol/LCuSO4��Һ��
(3)��4 mol/L������ͭ��Һϡ��������Һ�����ʵ�鲽���У�
a.���ձ��м���Լ100 mLˮ���г���ϡ�ͣ���ȴ������
b.����Ͳ��ȡһ�����4 mol/L������ͭ��Һ��һ�ձ���
c.��������4 mol/L����ͭ��Һ�����
d.�Ǻ�ƿ�����������µߵ�ҡ�Ⱥ���Һת�����Լ�ƿ��
e.��ˮ��Һ��������ƿ�̶���1~2 cm�����ý�ͷ�ιܽ��ж���
f. ϴ���ձ��Ͳ�����2~3�β���ϴ��Һע������ƿ������ҡ������ƿ��ʹ��Һ��Ͼ���
g. ����Һת��������ƿ
������ȷ�IJ���˳��Ϊ______________________��
(4)ָ�����ƹ����е��������ζ�������ҺŨ�ȵ�Ӱ��(�ƫ�ߡ���ƫ�͡�����Ӱ�족)��
��d����ҡ�Ⱥ���Һ����ڿ̶��ߣ��ټ�ˮ���̶��ߣ�___________��
��e�����У����ӿ̶��ߣ�___________��
��g����ǰ������ƿδ�������������ˮ��___________��
���𰸡�
(1)250 mL����ƿ ����Ƿ�©Һ
(2)12.5 12.5
(3)cbagfed
(4)��ƫ�� ��ƫ�� ����Ӱ��
��������
(1)����Ҫ0.2 mol/L CuSO4��Һ250 mL��������Ҫ250 mL ����ƿ��ʹ�ø�����ǰ������еIJ�����Ҫ����Ƿ�©Һ��
(2)CuSO4�����ʵ���n=cV= 0.2 mol��L1�� 0.25 L = 0.05 mol��CuSO4��5H2O�����ʵ�������CuSO4�����ʵ���������CuSO4��5H2O������Ϊ0.05 mol�� 250 g/ mol =12.5 g�������4 mol/L��CuSO4��Һϡ�����ƣ�������Ͳ��ȡ4 mol/L CuSO4��Һ�����Ϊ![]() =0.012 5 L��Ϊ12.5 mL��
=0.012 5 L��Ϊ12.5 mL��
(3)��4 mol/L������ͭ��Һ����250 mL 0.2 mol/L������ͭ��Һ�IJ���Ϊ�����㡢��ȡ��ϡ�͡���ȴ����Һ��ϴ�ӡ����ݡ�ҡ�ȣ�������ȷ�IJ���˳��Ϊ��cbagfed��
(4)�����ݺ�����ƿ������ҡ�ȣ����ú�Һ�治���̶��ߣ�����Ϊ������Һ������ƿ����ƿ��֮�䣬�ټ�ˮ���̶��ߣ�������Һ�����ƫ����ҺŨ��ƫ�ͣ�
������ʱ���ӿ̶��ߣ�����������Һ�����ƫС����ҺŨ��ƫ�ߣ�
����Һ�������ˮ���ݣ�����ƿδ���T����������Һ����������ҺŨ����Ӱ�졣

����Ŀ��������ǻ�����Ⱦ֯��ҽҩ��Ƥ��ȹ�ҵԭ�ϡ�ij���Ṥ�����ø���ƷY����β��SO2�õ�CaSO4���������ڵĺϳɰ����������Ʊ�(NH4)2SO4�������������£�
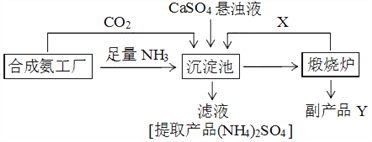
��ش��������⣺
��1�������й�(NH4)2SO4��Һ��˵����ȷ����_____
A�����뷽��ʽ:(NH4)2SO4![]() 2NH4++SO42-
2NH4++SO42-
B��ˮ�����ӷ���ʽ��NH4++H2O![]() NH3H2O+H+
NH3H2O+H+
C������Ũ�ȹ�ϵ��c(NH4+)+c(H+)=c(SO42-)+c(OH�C)
D����Ũ�ȴ�С��c(NH4+)>c(SO42-)>c(H+)>c(NH3H2O)>c(OH�C)
��2�����Ṥҵ�У�V2O5������ʱ������Ӧ2SO2+ O2 ![]() 2SO3��SO2��ת�������¶ȡ�ѹǿ�йأ�������±���Ϣ����Ϲ�ҵ����ʵ�ʣ�ѡ���±�������ʵ��¶Ⱥ�ѹǿ�ֱ���__________���÷�Ӧ420��ʱ��ƽ�ⳣ��_____520��ʱ��ƽ�ⳣ�����>������<����=������
2SO3��SO2��ת�������¶ȡ�ѹǿ�йأ�������±���Ϣ����Ϲ�ҵ����ʵ�ʣ�ѡ���±�������ʵ��¶Ⱥ�ѹǿ�ֱ���__________���÷�Ӧ420��ʱ��ƽ�ⳣ��_____520��ʱ��ƽ�ⳣ�����>������<����=������
| 1.01��105Pa | 5.05��105Pa | 1.01��106Pa |
420�� | 0.9961 | 0.9972 | 0.9984 |
520�� | 0.9675 | 0.9767 | 0.9852 |
620�� | 0.8520 | 0.8897 | 0.9276 |
��3����2L�ܱ�������ģ��Ӵ����Ʊ���������ʱ������12����ǡ�ôﵽƽ�⣬�������SO3�����ʵ���Ϊ1.2mol������ǰ12������������ʾ��Ӧ����v(O2)Ϊ___________��
��4������ƷY��__���������з�������Ҫ��Ӧ����ʽ��___________________��
��5������ɫ��ѧ����Դ�ۺ����õĽǶ�˵���������̵���Ҫ�ŵ���________________��






