题目内容
【题目】CO2 和CH4是常见的化合物,同时也是常用的化工原料。
Ⅰ.以CO2与NH3为原料可以合成尿素[CO(NH2)2]。合成尿素的反应为2NH3(g) + CO2(g) ![]() CO(NH2)2(s) + H2O(g)。
CO(NH2)2(s) + H2O(g)。
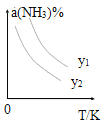
(1)在不同温度及不同y值下合成尿素,达到平衡时,氨气转化率变化情况如图所示。
①该反应的ΔH_____0(填“>” 或、“<” ),该反应自发进行的条件是_______________ (填“低温”“高温”或“任意温度”) 若y表示反应开始时的氨碳比[![]() ],则y1________y2。(填“>”、“<”或“=”);
],则y1________y2。(填“>”、“<”或“=”);
(2)t℃时,若向容积固定的密闭容器中加入一定量的 NH3和CO2合成尿素,下列叙述能说明此反应达到平衡状态的是________ (填字母)。
a.混合气体的平均相对分子质量保持不变
b.CO2和NH3的体积分数保持不变
c.CO2和NH3的转化率相等
d.混合气体的密度保持不变
e.1molCO2生成的同时有 2molN—H键断裂
II.工业上用CH4与水蒸气在一定条件下制取H2,:CH4(g) + H2O(g) ![]() CO(g) + 3H2(g) ΔH = + 203 kJmol-1
CO(g) + 3H2(g) ΔH = + 203 kJmol-1
①该反应逆反应速率表达式为:v逆=kc(CO) c3(H2),k 为速率常数,在某温度下测得实验数据如表:
CO浓度(molL-1) | H2浓度(molL-1) | 逆反应速率(molL-1min-1) |
0.05 | c1 | 4.8 |
c2 | c1 | 19.2 |
c2 | 0.1 | 8.1 |
由上述数据可得该温度下,该反应的逆反应速率常数k为____L3mol-3min-1。
②某温度下,在体积为3 L的密闭容器中通入物质的量均为3 mol的CH4和水蒸气,发生上述反应,5分钟时达到平衡,此时H2的体积分数为60%,则在5分钟内用CH4浓度变化表示的平均反应速率v(CH4)=________;该温度下该反应的平衡常数K=________。平衡后再向容器中加入1 mol CH4和1 mol CO,平衡_______移动(填“正反应方向”或“逆反应方向”或“不”)。
III.在常温下,将0.02mol CO2通入200mL 0.15mol/L的/span>NaOH溶液中,充分反应后下列关系式中正确的是_____________________
A.c(Na+)>c(HCO3-)> c(CO32-)>c(OH-)>c(H+)
B.3c (Na+)=2[c(CO32-)+ c(HCO3-)+ c(H2CO3)]
C.c (Na+)+c(H+)=c(HCO3-)+ c(CO32-)+c(OH-)
D.c(HCO3-)+ 3c(H2CO3)+2c(H+)= c(CO32-)+2c(OH-)
【答案】< 低温 < abd 40500 ![]() mol L-1min-1 48 正反应方向 AD
mol L-1min-1 48 正反应方向 AD
【解析】
Ⅰ、(1)通过图象分析温度升高,氨气转化率的变化从而分析反应吸放热;自发进行的判断依据是△H-T△S<0,结合反应特征分析判断需要的条件;若y表示反应开始时的水碳比,升温平衡逆向进行,氨气转化率减小,一定温度下,水和二氧化碳之比越大,平衡逆向进行,氨气转化率越小,则y1小于y2;
(2)平衡时是正逆反应速率相同,各组分含量保持不变,原则是变量不变分析选项;
II.①根据v逆=kc(CO)c3(H2)计算k的值;
②根据![]() 求出反应速率;根据
求出反应速率;根据![]() 计算平衡常数;通过浓度商与平衡常数的比较判断反应移动方向;
计算平衡常数;通过浓度商与平衡常数的比较判断反应移动方向;
III.可能发生的反应:CO2+2NaOH=Na2CO3+H2O、CO2+NaOH=NaHCO3,NaOH的物质的量为0.2L×0.15mol/L=0.03mol,先分析0.02mol CO2通入之后溶液的溶质,再进行判断;
Ⅰ、(1)图象分析得到温度升高,氨气转化率减小说明平衡逆向进行,正反应为放热反应,所以ΔH<0;自发进行的判断依据是△H-T△S<0,该反应ΔH<0,△S<0,所以需要低温条件才能自发进行;压强越大平衡正向进行,氨气转化率增大,若y表示压强,则一定温度下y1大于y2,若y表示反应开始时的水碳比,升温平衡逆向进行,氨气转化率减小,一定温度下,水和二氧化碳之比越大,平衡逆向进行,氨气转化率越小,则y1小于y2;
故答案为:<;低温;<;
(2)a.生成物有固体,利用极限法考虑,反应初始和彻底进行平均相对分子质量不同,混合气体的平均相对分子质量保持不变时说明平衡不再移动,故正确;
b.反应达到平衡各组分体积分数不变,CO2和NH3的体积分数保持不变说明平衡,故正确;
c.反应加入一定量的 NH3和CO2,若按2:1加入,则二者转化率始终相等,若不按2:1加入,二者转化率不可能相等,故CO2和NH3的转化率相等不能说明平衡,故错误;
d.混合气体体积不变,平衡右移时有固体生成,气体体积减小,即密度减小,所以混合气体的密度保持不变说明反应平衡,故正确;
e.一个氨气分子中有3个N—H键,2molN—H键断裂即2/3mol氨气反应,1molCO2生成的同时有 2molN—H键断裂时正反应速率和逆反应速率不相等,故错误;
故答案为:abd;
(3)①根据v逆=kc(CO)c3(H2),由表中数据,c13=![]() mol3/L3,则c2=
mol3/L3,则c2=![]() mol/L=0.2mol/L,所以k=
mol/L=0.2mol/L,所以k=![]() L3mol3min1=40500L3mol3min1,
L3mol3min1=40500L3mol3min1,
故答案为:40500;
②设转化的CH4为amol/L,容器体积为3L,则初始c(CH4)=3mol/3L=1mol/L,c(H2O)=3mol/3L=1mol/L,列三段式
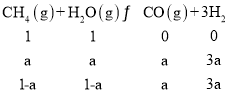
氢气的体积分数为![]() =60%,解得a=2/3mol/L,则v(CH4)=
=60%,解得a=2/3mol/L,则v(CH4)=![]() =
= ![]() mol L-1min-1;平衡常数
mol L-1min-1;平衡常数![]() =
=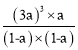 =48;平衡后再向容器中加入1 mol CH4和1 mol CO,此时浓度商Q=
=48;平衡后再向容器中加入1 mol CH4和1 mol CO,此时浓度商Q= ,所以反应向正反应方向移动,
,所以反应向正反应方向移动,
故答案为:40500;![]() mol L-1min-1;48;正反应方向;
mol L-1min-1;48;正反应方向;
III.可能发生的反应:CO2+2NaOH=Na2CO3+H2O、CO2+NaOH=NaHCO3,NaOH的物质的量为0.2L×0.15mol/L=0.03mol,1<n(NaOH):n(CO2)=3:2<2,则反应得到Na2CO3、NaHCO3混合溶液,设二者物质的量分别为xmol、ymol,则![]() ,解得x=y=0.01,即溶液中的溶质为Na2CO3和NaHCO3;
,解得x=y=0.01,即溶液中的溶质为Na2CO3和NaHCO3;
A.溶液显碱性,且碳酸根的水解程度大于碳酸氢根的电离程度,所以溶液中存在:c(Na+)>c(HCO3-)> c(CO32-)>c(OH-)>c(H+),A项正确;
B.根据物料守恒可知2c (Na+)=3[c(CO32-)+ c(HCO3-)+ c(H2CO3)],B项错误;
C.根据电荷守恒可知c (Na+)+c(H+)=c(HCO3-)+ 2c(CO32-)+c(OH-),C项错误;
D.电荷守恒和物流守恒联立消去钠离子即得c(HCO3-)+ 3c(H2CO3)+2c(H+)= c(CO32-)+2c(OH-)(质子守恒),故D项正确;
故答案为:AD。

 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案【题目】某实验小组探究AgNO3溶液与Na2SO3溶液的反应。
实验I | 操作 | 现象 |
| 滴加5滴0.1mol/L Na2SO3溶液,振荡 | 产生白色沉淀,测得混合溶液pH=5 |
继续滴加0.1mol/L Na2SO3溶液,振荡 | 白色沉淀增多,继续滴加,白色沉淀消失,测得混合溶液pH=9 |
资料:Ag2SO3,白色固体,难溶于水;Ag2SO4,白色固体,微溶于水;AgOH,白色固体,常温下不稳定,易分解产生棕褐色固体。
(1)测得0.1mol/L Na2SO3溶液pH=10,用离子方程式解释原因:_______。
(2)实验小组对白色沉淀的成分提出猜想:
①可能含Ag2SO3。
②可能含Ag2SO4,理由是________。
③可能含AgOH。
实验产生的白色沉淀放置一段时间后未发生明显变化,排除猜想③。
(3)检验白色沉淀的成分
(资料:Ag++2S2O32![]() Ag(S2O3)23,Ag(S2O3)23在溶液中稳定存在。)
Ag(S2O3)23,Ag(S2O3)23在溶液中稳定存在。)
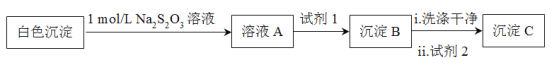
测得沉淀C质量小于沉淀B,试剂1和试剂2分别是_____、______,说明白色沉淀是Ag2SO3和Ag2SO4的混合物。
(4)探究白色沉淀消失的原因。实验小组设计对照实验:
实验II | 实验III | |
实验操作 |
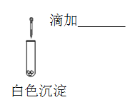
|
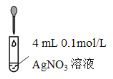
|
现象 | 沉淀溶解 |
① 补充实验III的实验操作及现象:_______,证明SO32使白色沉淀溶解。
② 查阅资料:Ag2SO3能溶于过量Na2SO3溶液中形成Ag(SO3)23。白色沉淀中含有g2SO4,但还能全部溶解于Na2SO3溶液的原因是______。
(5)探究AgNO3溶液与Na2SO3溶液能否发生氧化还原反应。
实验IV | 操作 | 现象 |
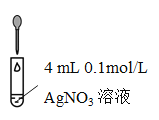
| 步骤i:滴加一定体积0.1 mol/L Na2SO3溶液 | 产生白色沉淀 |
步骤ii:再加入NaOH溶液调pH=14,振荡 | 白色沉淀变黑,经检验为Ag |
步骤ii中Ag2SO3发生反应的离子方程式是_________。
(6)综合实验I和IV,说明AgNO3溶液与Na2SO3溶液的反应类型与_______有关。