��Ŀ����
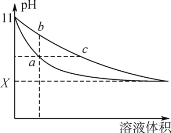
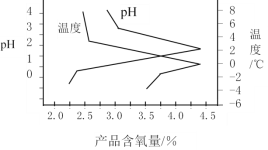
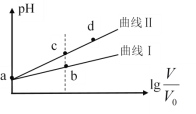
����Ŀ��ij�¶��£�HNO2��CH3COOH�ĵ��볣���ֱ�Ϊ5.0��10-4��1.7��10-5����pH��ͬ�������ΪV0����������Һ�ֱ��ˮϡ�������V��pH��![]() �ı仯��ͼ��ʾ�����������������
�ı仯��ͼ��ʾ�����������������
A.����������CH3COOH��Һ
B.��Һ��ˮ�ĵ���̶ȣ�b��С��c��
C.��ͬ���a���������ֱ���NaOH��Һǡ���кͺ���Һ��n(NO2��)��n(CH3COO��)
D.��c�㵽d�㣬��Һ��![]() ���ֲ��䣨����HA��A���ֱ������Ӧ�����������ӣ�
���ֲ��䣨����HA��A���ֱ������Ӧ�����������ӣ�
���𰸡�C
��������
�ɵ��볣����֪��HNO2��CH3COOH�������ᣬ���Ҵ�������Ը�����pH��ͬ�������ΪV0����������Һ�У���������ʵ������������
A. ��ͬpH�������ˮϡ�ͣ�����Խǿ���ᣬpH�仯Խ����������������CH3COOH��Һ����ȷ��
B.��ͼ�п��Կ�������Һ��pH b��С��c�㣬˵��c(H+)b���c���c(OH-) c���b��Ӷ�˵����Һ��ˮ�ĵ���̶�c���b�����ȷ��
C. ��ͬ���a��������ᣬ��������ʵ����ֱ���NaOH��Һǡ���кͺ���Һ��n(NO2��)<n(CH3COO��)������
D. ��c�㵽d�㣬����ĵ��볣����ˮ�ĵ��볣�������䣬����Kw/Ka���䣬��![]() ���ֲ��䣬��ȷ��
���ֲ��䣬��ȷ��
�ʴ�ΪC��

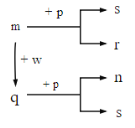
����Ŀ��TKʱ����2.0 L�����ܱ������г���0.10 mol COCl2��������ӦCOCl2(g)![]() Cl2(g)+CO(g)������һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ�IJ������ݼ��±���
Cl2(g)+CO(g)������һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ�IJ������ݼ��±���
t/s | 0 | 2 | 4 | 6 | 8 |
n(Cl2)/mol | 0 | 0.030 | 0.039 | 0.040 | 0.040 |
����˵����ȷ����
A. ���������������䣬�����¶ȣ�ƽ��ʱc(Cl2)=0.022 mol��L-1����Ӧ����H<0
B. ��Ӧ��ǰ2 s��ƽ������v(CO)=0.015 mol��L-1��s-1
C. ���������������䣬��ʼ�������г���0.12 mol COCl2��0.06 mol Cl2��0.06 mol CO����Ӧ�ﵽƽ��ǰ�����ʣ�v��<v��
D. ���������������䣬��ʼ�������г���0.10 mol Cl2��0.08 mol CO���ﵽƽ��ʱ��Cl2��ת����С��60%