题目内容
【题目】葡萄糖酸亚铁[(C6H11O7)2Fe2H2O]是重要的矿物质添加剂,它的吸收效果比无机铁盐好。一种工业上制备葡萄糖酸亚铁的工艺流程如下:
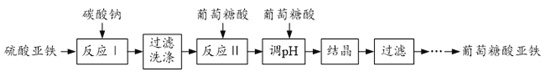
(1)反应Ⅰ的化学方程式为______。
(2)①碳酸亚铁过滤时需在表面保留水层的原因是______;
②检验FeCO3已经洗涤干净的操作为______。
(3)反应Ⅱ后加入葡萄糖酸调节溶液pH至5.8,其原因是______。
(4)葡萄糖酸亚铁溶液结晶、洗涤时均需加入乙醇,其目的分别是______,______。
【答案】 FeSO4+Na2CO3=FeCO3↓+Na2SO4 隔绝空气,防止氧化 取最后一次洗涤液,向其中加入BaCl2溶液无沉淀生成 防止Fe2+的水解 降低溶剂的极性,使晶体更易析出 减少产品在洗涤时的损失且更易干燥
【解析】(1)反应Ⅰ是硫酸亚铁和碳酸钠发生的复分解反应,反应的化学方程式为FeSO4+Na2CO3=FeCO3↓+Na2SO4,故答案为:FeSO4+Na2CO3=FeCO3↓+Na2SO4;
(2)①碳酸亚铁中的亚铁离子容易被空气中的氧气氧化,为了避免被氧化,过滤时需在表面保留水层,故答案为:隔绝空气,防止氧化;
②FeCO3沉淀表面吸附有少量硫酸钠,检验碳酸亚铁洗涤干净只需要具有上面不再附有硫酸根离子即可,方法为取最后一次洗涤液,向其中加入BaCl2溶液,若无沉淀生成,则说明已经洗涤干净,故答案为:取最后一次洗涤液,向其中加入BaCl2溶液无沉淀生成;
(3)反应Ⅱ后加入葡萄糖酸调节溶液pH至5.8,主要是防止Fe2+的水解,故答案为:防止Fe2+的水解;
(4)葡萄糖酸亚铁溶液结晶、洗涤时均需加入乙醇,乙醇可以降低溶剂的极性,使晶体更易析出,减少产品在洗涤时的损失,另外乙醇容易挥发,使得晶体更易干燥,故答案为:降低溶剂的极性,使晶体更易析出;减少产品在洗涤时的损失且更易干燥。

 黄冈创优卷系列答案
黄冈创优卷系列答案