题目内容
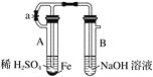
【题目】关于电解池应用的规律提炼题组某化学兴趣小组用下图所示装置进行电化学原理的实验探究,回答下列问题:
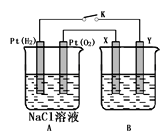
(1)通O2的Pt电极为电池__________极(填电极名称),其电极反应式为______________。
(2)若B电池为电镀池,目的是在某镀件上镀一层银,则X电极材料为_________,电解质溶液为__________。
(3)若B电池为精炼铜,且粗铜中含有Zn、Fe、Ag、Au等杂质,在__________电极(填“X”或“Y”)周围有固体沉积成阳极泥,阳极泥的成分为___________。
(4)若X、Y均为Pt,B电池的电解质溶液为500 mL 1.0mol/L的NaCl溶液,当电池工作一段时间断开电源K,Y电极有560mL(标准状况)无色气体生成(假设电极产生气体完全逸出,溶液体积不变)。恢复到常温下,B电池溶液的pH=___________,要使该溶液恢复到原来的状态,需加入__________(填物质并注明物质的量)。
(5)若X、Y均是铜,电解质溶液为NaOH溶液,电池工作一段时间,X极附近生成砖红色沉淀,查阅资料得知是Cu2O,试写出该电极发生的电极反应式为_______________。
(学法题)通过以上题目,请总结书写电极反应式的关键____________ 。
【答案】 正 O2+4e-+2H2O=4OH- Ag AgNO3溶液 X Ag、Au 13 0.05molHCl 2Cu-2e-+2OH-=Cu2O+H2O 电池的判断、电极是活性电极还是惰性电极及电解质溶液中的离子放电先后顺序(其他答案合理也给分)。
【解析】试题分析:(1)装置A是氢氧燃料电池,氧气发生还原反应,所以通入氧气的电极是正极;(2)电镀时,镀件作阴极、镀层金属作阳极、含有镀层金属的盐作电解质;(3)电解法精炼铜,粗铜作阳极、精铜作阴极,粗铜中铜及活泼性大于铜的金属失电子,活泼性小于铜的金属不能失电子;(4)Y极是阴极,发生还原反应生成氢气,Y电极有560mL(标准状况)氢气生成,根据电解方程式计算溶液的pH,根据放出气体的物质的量分析要使该溶液恢复到原来的状态需加入的物质。(5)根据题目信息,X极是铜失电子生成Cu2O。
解析:(1)装置A是氢氧燃料电池,氧气发生还原反应,所以通入氧气的电极是正极;在中性溶液中氧气得电子生成氢氧根离子,电极反应式为O2+4e-+2H2O=4OH-;(2)电镀时,镀件作阴极、镀层金属作阳极、含有镀层金属的盐作电解质,X与正极相连,X是阳极,所以X电极材料为Ag,电解质溶液为AgNO3溶液。(3)电解法精炼铜,粗铜作阳极、精铜作阴极,粗铜中铜及活泼性大于铜的金属失电子,活泼性小于铜的金属不能失电子,X是阳极,所以在X极周围有固体沉积成阳极泥,Ag、Au的活泼性小于铜,所以阳极泥的成分为Ag、Au;(4)Y极是阴极,发生还原反应生成氢气,Y电极有560mL(标准状况)氢气生成,生成氢气的物质的量是0.025mol,设生成氢氧化钠的物质的量是xmol、生成氯气的物质的量是ymol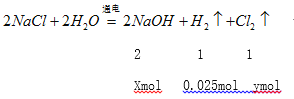
X=0.05mol、y=0.025mol;B池溶液氢氧化钠的浓度是![]() ,所以pH=13;由于反应放出0.025mol氢气和0.025mol氯气,所以要使该溶液恢复到原来的状态,需加入0.05molHCl;
,所以pH=13;由于反应放出0.025mol氢气和0.025mol氯气,所以要使该溶液恢复到原来的状态,需加入0.05molHCl;
(5)根据题目信息,X极是铜失电子生成Cu2O,电极反应为:2Cu-2e-+2OH-=Cu2O+H2O。
书写电极反应式的关键:电极的判断、电极是活性电极还是惰性电极及电解质溶液中的离子放电先后顺序。