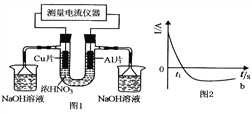
题目内容
【题目】锡是大名鼎鼎的“五金”——金、银、铜、铁、锡之一,早在远古时代,人们便发现并使用了锡。回答下列问题:
(1)锡是50号元素,在元素周期表中位于________区。
(2)SnO2是一种重要的半导体传感器材料,用来制备灵敏度高的气敏传感器,SnO2与熔融NaOH反应生成Na2SnO3,Na2SnO3中阴离子的空间构型为________。
(3)比较下列卤化锡的熔点和沸点,分析其变化规律及原因____________________________________
SnCl4 | SnBr4 | SnI4 | |
熔点/℃ | -33 | 31 | 144.5 |
沸点/℃ | 114.1 | 202 | 364 |
(4)汽车废气中常含有有毒的一氧化碳气体,但在二氧化锡的催化下,在300 ℃时,一氧化碳可大部分转化为二氧化碳。C、O、Sn电负性由大至小的顺序是__________________________________________。
(5)灰锡具有金刚石型结构,其中Sn原子的杂化方式为________,微粒之间存在的作用力是__________________________________。
(6)①原子坐标参数,表示晶胞内部各原子的相对位置,如图为灰锡的晶胞,其中原子坐标参数A为(0,0,0),B为(1/2,0/1/2),则D为(1/4,___ ,___ )。锡的配位数为________。

②已知灰锡的晶胞参数a=0.648 9 nm,其密度为______ g·cm-3(NA为6.02×1023 mol-1,不必算出结果,写出简化后的计算式即可)。
【答案】p 平面三角形 SnCl4、SnBr4、SnI4熔沸点依次升高;原因是它们分子结构相似,随相对分子质量增大,分子间相互作用力逐渐增强 O>C>Sn sp3杂化 非极性共价键(或共价键) 1/4 1/4 1 8×118.7/(6.02×648.93)×107
【解析】
(1)锡的价电子排布式为5s25p2;
(2)SnO32—中Sn原子的价层电子对数为3,孤对电子数为0;
(3)SnCl4、SnBr4、SnI4均为分子晶体,结构相似的分子晶体,随着相对分子质量的增大,分子间作用力依次增大;
(4)元素的非金属性越强,电负性越大;
(5)①由晶胞结构可知,A为与立方体的顶点、B位于面心、D位于体对角线的1/4处;
②晶胞中含有的Sn原子个数是8×1/8+6×1/2+4=8,依据公式计算晶胞的密度。
(1)锡是50号元素,位于周期表第五周期ⅣA族,价电子排布式为5s25p2,则在元素周期表中位于p区,故答案为:p;
(2)SnO32—中Sn原子的价层电子对数为3,孤对电子数为0,则SnO32—中Sn原子为sp2杂化,SnO32—的空间构型为平面三角形,故答案为:平面三角形;
(3)由表格数据可知,SnCl4、SnBr4、SnI4均为分子晶体,熔沸点依次升高;结构相似的分子晶体,随着相对分子质量的增大,分子间作用力依次增大,溶沸点依次增大,故答案为:nCl4、SnBr4、SnI4熔沸点依次升高;它们分子结构相似,随相对分子质量增大,分子间相互作用力逐渐增强;
(4)元素的非金属性越强,电负性越大,非金属性的强弱顺序为O>C>Sn,则电负性由大至小的顺序为O>C>Sn,故答案为:O>C>Sn;
(5)由于灰锡具有金刚石型结构,则Sn原子的杂化方式为sp3杂化,由于灰锡由同一元素的原子通过共用电子对结合而成,所以微粒之间存在的作用力是非极性共价键,故答案为:4;非极性共价键;
(6)①由晶胞结构可知,A为与立方体的顶点、B位于面心、D位于体对角线的1/4处,所以其坐标参数是(1/4,1/4,1/4),故答案为:1/4;1/4;
②根据晶胞结构可知,在晶胞中含有的Sn原子个数是8×1/8+6×1/2+4=8,所以晶胞的密度为8×118.7/(6.02×648.93)×107g·cm-3,故答案为:8×118.7/(6.02×648.93)×107。

 发散思维新课堂系列答案
发散思维新课堂系列答案【题目】N2O5是一种新型硝化剂,在一定温度下可发生如下反应:2N2O5(g) ![]() 4NO2(g)+O2(g) ΔH>0。T1温度时,向密闭容器中通入N2O5气体,部分实验数据见下表:
4NO2(g)+O2(g) ΔH>0。T1温度时,向密闭容器中通入N2O5气体,部分实验数据见下表:
时间/s | 0 | 500 | 1 000 | 1 500 |
c(N2O5)/ mol·L-1 | 5.00 | 3.52 | 2.50 | 2.50 |
下列说法正确的是
A. 500 s内NO2的生成速率为2.96×10-3 mol·L-1·s-1
B. T1温度下该反应平衡时NO2的产率为25%
C. 达到平衡后,其他条件不变,将容器的体积压缩到原来的1/2,则c(N2O5)<5.00 mol·L-1
D. T1温度下的平衡常数为K1,T2温度下的平衡常数为K2,若T1>T2,则K1>K2
【题目】硫酸是重要的化工原料,生产过程中SO2催化氧化生成SO3的化学反应为:2SO2(g)+O2(g) ![]() 2SO3(g)。
2SO3(g)。
(1)实验测得SO2反应生成SO3的转化率与温度、压强有关,请根据下表信息,结合工业生产实际,选择最合适的生产条件是________。
压强 SO2转化率 温度 | 1个大气压 | 5个大气压 | 10个大气压 | 15个大气压 |
400℃ | 0.9961 | 0.9972 | 0.9984 | 0.9988 |
500℃ | 0.9675 | 0.9767 | 0.9852 | 0.9894 |
600℃ | 0.8520 | 0.8897 | 0.9276 | 0.9468 |
(2)反应2SO2(g)+O2(g) ![]() 2SO3(g)达到平衡后,改变下列条件,能使SO2(g)平衡浓度比原来减小的是________(填字母)。
2SO3(g)达到平衡后,改变下列条件,能使SO2(g)平衡浓度比原来减小的是________(填字母)。
A.保持温度和容器体积不变,充入1molO2(g)
B.保持温度和容器体积不变,充入2mol SO3(g)
C.降低温度
D.在其他条件不变时,减小容器的容积
(3)某温度下, SO2的平衡转化率(α)与体系总压强(P)的关系如下图所示。
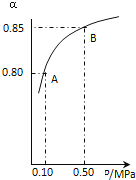
2.0 molSO2和1.0mol O2置于10L密闭容器中,反应达平衡后,体系总压强为0.10 MPa。平衡状态由A变到B时,平衡常数K(A)_____K(B)(填“>”、“<”或“=”), B点的化学平衡常数是______。
(4)在一个固定容积为5L的密闭容器中充入0.20mol SO2和0.10molO2, t1时刻达到平衡,测得容器中含SO30.18mol。
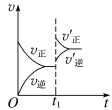
①tl 时刻达到平衡后,改变一个条件使化学反应速率发生如下图所示的变化,则改变的条件是________。
A.体积不变,向容器中通入少量O2
B.体积不变,向容器中通入少量SO2
C.缩小容器体积
D.升高温度
E.体积不变,向容器中通入少量氮气
②若继续通入0.20mol SO2和0.10molO2,则平衡________移动(填“向正反应方向”、“向逆反应方向”或“不”) ,再次达到平衡后,n(SO3)的取值范围是_____________。