题目内容
3.下列说法正确的是( )| A. | 在化学反应中,原子重新组合时伴随着能量的变化 | |
| B. | 淀粉和纤维素的化学式均为(C6H10O5)n,故互为同分异构体 | |
| C. | 通过化学变化可以“点石成金”,即可将黏土转化成金单质 | |
| D. | 等质量的铝粉按a、b两种途径完全转化,途径a比途径b消耗更多的NaOH 途径a:Al$→_{点燃}^{O_{2}}$Al2O3$\stackrel{NaOH溶液}{→}$NaAlO2;途径b:Al$\stackrel{NaOH溶液}{→}$NaAlO2 |
分析 A.化学反应的过程从微粒角度考虑就是原子重新组合过程;
B.纤维素和淀粉的化学成分均为(C6H10O5)n,但两者的n不同;
C.化学反应的最小微粒是原子;
D.化学反应的热效应只与反应物的初始状态和生成物的最终状态有关.
解答 解:A.化学反应的过程从微粒角度考虑就是原子重新组合过程,断键吸收能量,成键放出能量,故A正确;
B.纤维素和淀粉的化学成分均为(C6H10O5)n,但两者的n不同,所以两者的分子式不同,不是同分异构体,故B错误;
C.化学反应的最小微粒是原子,不可能生成金单质,故C错误;
D.化学反应的热效应只与反应物的初始状态和生成物的最终状态有关,故ab两种途径,放出的热量一样多,故D错误.
故选A.
点评 本题考查同分异构体的判断、化学反应的热效应、化学变化等,综合性较强,难度难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.下列对“物质的量”的叙述正确的是( )
| A. | 物质的量就是物质的质量 | |
| B. | 物质的量不是国际单位制的七个基本物理量之一 | |
| C. | 物质的量是摩尔的单位 | |
| D. | 阿伏加德罗常数的数值约为6.02×1023 |
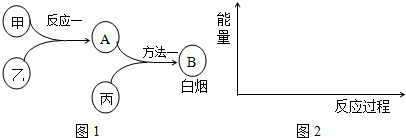
8.已知甲、乙、丙是中学常见的三种气体单质,相互间反应可制得化肥B.其转化关系如图1所示:
ⅠAⅡAⅢAⅣAⅤAⅥAⅦA0周期族
(1)将B中所含元素填写在如表的恰当位置中(用元素符号表示)
(2)已知反应一是放热反应,画出能量关系示意图2.
(3)为加快反应一的速率,可采取的措施有:适当升高温度、选用恰当的催化剂、增大某一反应物的浓度和增大压强.
(4)方法一的化学方程式是3Cl2+8NH3=N2+6NH4Cl.
(5)用方法二也能制得B:甲和丙反应的产物与A反应即可,这两种方法更好的是方法二(填“方
法一”或“方法二”),理由是方法二的原子利用率100%,零排放,符合绿色化学理念.

ⅠAⅡAⅢAⅣAⅤAⅥAⅦA0周期族
(1)将B中所含元素填写在如表的恰当位置中(用元素符号表示)
| 1 | ||||||||
| 2 | ||||||||
| 3 |
(3)为加快反应一的速率,可采取的措施有:适当升高温度、选用恰当的催化剂、增大某一反应物的浓度和增大压强.
(4)方法一的化学方程式是3Cl2+8NH3=N2+6NH4Cl.
(5)用方法二也能制得B:甲和丙反应的产物与A反应即可,这两种方法更好的是方法二(填“方
法一”或“方法二”),理由是方法二的原子利用率100%,零排放,符合绿色化学理念.
15.一定温度下,在一容积不变的密闭容器中发生的可逆反应2X(g)?Y(g)+Z (s),以下不能作为反应达到平衡标志的是( )
| A. | X的分解速率是Y的消耗速率 的2倍 | |
| B. | 混合气体的压强不再变化 | |
| C. | 混合气体的密度不再变化 | |
| D. | 单位时间内生成lmolY的同时分解2mol X |
12.下列关于0.2mol/LNaHCO3溶液的说法正确的是( )
| A. | 溶质电离方程式为NaHCO3═Na++H++CO32- | |
| B. | 25℃时,加水稀释后,n(H+)与n(OH-)的乘积变大 | |
| C. | 离子浓度关系:c(Na+)+c(H+)=c(OH-)+c(HCO3-)+c(CO32-) | |
| D. | 温度升高,c(HCO3-)增大 |
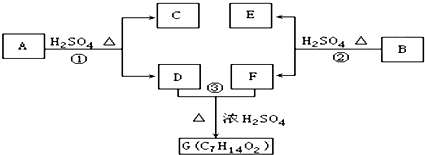
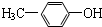 ;
;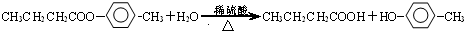 ;
;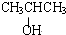 ;写出生成G的化学方程式CH3CH2CH2COOH+
;写出生成G的化学方程式CH3CH2CH2COOH+