题目内容
14.A、B、C、D、E都是短周期元素,原子序数依次增大,A、B处于同一周期,C、D、E同处另一周期.C、B可按原子个数比2:l和1:1分别形成两种离子化合物甲和乙.A原子的最外层电子数比次外层电子层多3个.E是地壳中含量最高的金属元素.根据以上信息回答下列问题:
(1)D元素在周期表中的位置是第三周期ⅡA族,乙物质的电子式是
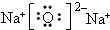 .
.(2)B、C、D、E四种元素的简单离子半径由大到小的顺序是(用离子符号填写)O2-<Na+<Mg2+<Al3+.
(3)E的单质加入到C的最高价氧化物对应的水化物的溶液中,发生反应的离子方程式是2Al+2OH-+2H2O═2AlO2-+3H2↑.
(4)简述比较D与E金属性强弱的实验方法:分别把两金属放入盛有少量水的试管中,并加入一段时间,再向两试管中滴加几滴酚酞试剂,放入Mg的试管变红,放入Al的试管不变色,说明Mg的金属性比Al强.
分析 A、B、C、D、E都是短周期元素,原子序数逐渐增大,A原子的最外层电子数比次外层电子层多3个,原子只能有2个电子层,最外层电子数为5,故A为N元素;E是地壳中含量最高的金属元素,则E为Al;A、B处于同一周期,C、D、E同处另一周期,即A、B处于第二周期,C、D、E处于第三周期,C、B可按原子个数比2:l和1:1分别形成两种离子化合物甲和乙,则C是Na元素,B是O元素,甲是Na2O,乙是Na2O2,D的原子序数介于Na、Al之间,故D为Mg,据此答题.
解答 解:A、B、C、D、E都是短周期元素,原子序数逐渐增大,A原子的最外层电子数比次外层电子层多3个,原子只能有2个电子层,最外层电子数为5,故A为N元素;E是地壳中含量最高的金属元素,则E为Al;A、B处于同一周期,C、D、E同处另一周期,即A、B处于第二周期,C、D、E处于第三周期,C、B可按原子个数比2:l和1:1分别形成两种离子化合物甲和乙,则C是Na元素,B是O元素,甲是Na2O,乙是Na2O2,D的原子序数介于Na、Al之间,故D为Mg.
(1)D为Mg,处于周期表中第三周期ⅡA族,乙是Na2O2,电子式为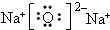 ,故答案为:第三周期ⅡA族;
,故答案为:第三周期ⅡA族;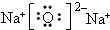 ;
;
(2)O2-、Na+、Mg2+、Al3+离子电子层结构相同,核电荷数越大离子半径越小,故离子半径:O2-<Na+<Mg2+<Al3+,故答案为:O2-<Na+<Mg2+<Al3+;
3)E的单质为Al,C的最高价氧化物对应的水化物为NaOH,二者反应生成偏铝酸钠与氢气,发生反应的离子方程式是:2Al+2OH-+2H2O═2AlO2-+3H2↑,
故答案为:2Al+2OH-+2H2O═2AlO2-+3H2↑;
(4)比较Mg与Al金属性强弱的实验方法:分别把两金属放入盛有少量水的试管中,并加入一段时间,再向两试管中滴加几滴酚酞试剂,放入Mg的试管变红,放入Al的试管不变色,说明Mg的金属性比Al强,
故答案为:分别把两金属放入盛有少量水的试管中,并加入一段时间,再向两试管中滴加几滴酚酞试剂,放入Mg的试管变红,放入Al的试管不变色,说明Mg的金属性比Al强.
点评 本题考查位置结构性质关系应用,元素的推断是答题的关键,注意金属性、非金属性强弱比较实验事实.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | 苯 | B. | 乙烯 | C. | 乙醇 | D. | KMnO4溶液 |
| A. | 若容器中X2全部转化为它的同素异形体X3,那么X3的分子量有3种 | |
| B. | 质量数为16的一种核素在此容器中的原子百分数为80% | |
| C. | 只要容器中同位素组成不变,X原子在任何条件下发生重新组合,最后得到三种X2,分子数之比总是15:4:1 | |
| D. | 此容器中X2的平均分子量是32.6 |
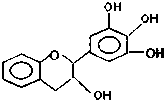 “茶倍健”牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂.其中没食子儿茶素(EGC)的结构如图所示.关于EGC的下列叙述中不正确的是( )
“茶倍健”牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂.其中没食子儿茶素(EGC)的结构如图所示.关于EGC的下列叙述中不正确的是( )| A. | EGC分子中所有的原子一定不共面 | |
| B. | 1mol EGC可以与2molBr2发生取代反应 | |
| C. | EGC可以发生氧化反应和取代反应,1mol该物质可以与6molH2发生加成反应 | |
| D. | 1molEGC与3molNa恰好完全反应 |
| A. | 分子的稳定性与化学键的强弱无关 | |
| B. | 参加反应的氢气和氧气的总能量高于反应生成水的总能量 | |
| C. | 断开参加反应的氢气和氧气中的化学键吸收的能量大于生成水时形成化学键放出的能量 | |
| D. | 该反应需要点燃,所以是吸热反应 |
| A. | 常温常压下,7.0g乙烯与丙烯的混合物中含有氢原子的数目为NA | |
| B. | 常温常压下,22.4 L CH4中含有的C-H键数为4NA | |
| C. | 含0.2 mol H2SO4的浓硫酸与足量Cu反应,生成SO2的分子数为0.1NA | |
| D. | lmol FeCl2与足量氯气反应时转移的电子数为2NA |
①Al(OH)3 ②NaHCO3 ③(NH4)2S ④NaHSO4.
| A. | 只有① | B. | ①和② | C. | ①②③ | D. | ①②③④ |