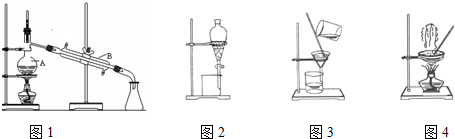
��Ŀ����
8��ӡˢ��·�ķϸ�ʴҺ���д���CuCl2��FeCl2��FeCl3�������ŷŽ����»�����Ⱦ����Դ���˷ѣ�������Ի������ã���FeCl3��Һ����ӡˢ��·���ķ�Һ�Ʊ�CuCl2•2H2O�Ĺ�����ͼ��
��1��֤������1����FeCl3��Һ�����ķ�����ȡ����1��Ӧ�����Һ���Թ��У��μ�KSCN��Һ����������Һ�ʺ�ɫ˵���Ȼ�����Һ������
��2������2���ӵ������������˵���B������ĸ����A��HNO3 B��H2O2 C��KMnO4
��3������3��Ŀ����ʹ��Һ��pH���ߵ�4.2����ʱFe3+��ȫ��������ѡ�õġ��Լ�1����CuO��д��һ�ּ��ɣ���
��4����֪�������ݣ�
| ���� | Fe��OH��2 | Cu��OH��2 | Fe��OH��3 |
| Ksp/25�� | 8.0��10-16 | 2.2��10-29 | 4.0��10-38 |
| ��ȫ����ʱ��pH��Χ | ��9.6 | ��6.4 | 3��4 |
A����û����Һ����μ���NaOH��Һ�����ȿ������ɫ����
B������Һ��c��Cl-����[c��Cu2+��+c��Fe2+��+c��Fe3+��]��7��3
C�������Һ�м���������ˮ��������pH��3��4����ˣ��ɻ�ô�����CuCl2��Һ
D����pH=5����Һ��Fe2+���ܴ�������
��5������Ũ��CuCl2��Һʱ��Ҫ�μ�Ũ���ᣬĿ����CuCl2��Һˮ������������ͭ�����ᣬCuCl2+2H2O?Cu��OH��2+2HCl���μ�Ũ���������Ȼ�ͭ��ˮ�⣨�û�ѧ����ʽ��ϼ�Ҫ������˵�������پ���ȴ���ᾧ�����ˣ��õ�CuCl2•2H2O��
���� ��FeCl3��Һ����ӡˢ��·���ķ�Һ��ӡˢ��·�ķϸ�ʴҺ���д���CuCl2��FeCl2��FeCl3������Cu2+��Fe2+��Fe3+���ӣ���Һ�м���������������������Ϊ�����ӣ���������ͭ������ҺPHʹ������ȫ�����������˵õ��Ȼ�ͭ��Һ��ͨ��Ũ����������ȴ�ᾧ������ϴ�ӣ��õ�CuCl2•2H2O��ע������Ũ��CuCl2��Һʱ��Ҫ�μ�Ũ�����ֹͭ���ӵ�ˮ�⣬
��1����������������KSCN��Һ��仯Ϊ��ɫ��Ƽ��飻
��2������2���ӵ��������������������ӣ������������µ����ʣ�
��3������3��Ŀ����ʹ��Һ��pH���ߵ�4.2����ʱFe3+��ȫ������������ҺPH��ָ���������ʺ��ᷴӦ���Ҳ��������µ����ʣ�
��4��A������Ksp�Ĵ�С�ж��ܽ��ԣ�
B��Cu2+��Fe2+��Fe3+����ˮ�⣬������ǵ����ʵ�������٣�
C��������ˮ�����������ӵõ��Ȼ������Ȼ�ͭ�Ļ����Һ��������ҺPH���Գ�ȥ�Ȼ�����
D�������ܶȻ�����ͳ�����ȫ����ҺPH�����жϣ�
��5��CuCl2��Һˮ������������ͭ�����ᣬ����ʱ����ӷ����ٽ�ˮ��ƽ��������еõ�ˮ����
��� �⣺��1��֤������1����FeCl3��Һ�����ķ��������������ӵ��������ʣ��������������Һ���ɫ��ƣ�����Ϊ��ȡ����1��Ӧ�����Һ���Թ��У��μ�KSCN��Һ����������Һ�ʺ�ɫ˵���Ȼ�����Һ������
�ʴ�Ϊ��ȡ����1��Ӧ�����Һ���Թ��У��μ�KSCN��Һ����������Һ�ʺ�ɫ�Ȼ�����Һ������
��2������2���ӵ���������Ŀ���������������ӣ����ڳ�ȥ�Ҳ������µ����ʣ�ѡ����AC���������������ӣ��������������������ӣ���������ԭΪˮ�������������������ӣ���ѡB��
�ʴ�Ϊ��B��
��3������3��Ŀ����ʹ��Һ��pH���ߵ�4.2����ʱFe3+��ȫ������������ҺPH��ָ��������ʺ��ᷴӦ���Ҳ��������µ����ʣ�������CuO��Cu2��OH��2CO3�ȣ�
�ʴ�Ϊ��CuO��
��4��A���ӱ����п��Կ�����Fe��OH��3��Ksp����С�ģ����������ȳ��ֳ�������A��ȷ��
B����ΪCu2+��Fe2+��Fe3+��Ӧ�ļ�ȫ�����������������������Һ�ж��ᷢ��ˮ�⣬������ǵ����ʵ�������٣���B��ȷ��
C��������ˮ��������������ȫ���������ۣ������ڵ���pHʱ������Լ�Ҳ������Һ�������������ɻ�ô�����CuCl2��Һ����C��ȷ��
D����pH=5����Һ��c��H+��=10-5moL/L��c��Fe3+��=$\frac{4��1{0}^{-38}}{��1��1{0}^{-5}��^{3}}$mol/L=4��10-13mol/L��Fe3+���ܴ������ڣ�c��Fe2+��=$\frac{8.0��1{0}^{-16}}{��1��1{0}^{-5}��^{2}}$=8.0��10-6mol/L����֪Fe2+�ܴ������ڣ���D����
��ѡABC��
��5��CuCl2��Һˮ������������ͭ�����ᣬ����ʱ����ӷ����ٽ�ˮ��ƽ��������еõ�ˮ��������Ũ��CuCl2��Һʱ��Ҫ�μ�Ũ�����Ƿ�ֹͭ���ӵ�ˮ�⣬
�ʴ�Ϊ��CuCl2��Һˮ������������ͭ�����ᣬCuCl2+2H2O?Cu��OH��2+2HCl���μ�Ũ���������Ȼ�ͭ��ˮ�⣮
���� ���⿼�����ܵ���ʵ��ܽ�ƽ���Լ�ת����֪ʶ����Ŀ�Ѷ��еȣ�ע�������ˮ�������ʣ�ע�����������ԵıȽϣ�ע���ܶȻ��ļ��㹫ʽ�����ã�

 ѧϰʵ����ϵ�д�
ѧϰʵ����ϵ�д�| A�� | ��Ϊ̼�ᡢ��ˮ�ܹ����磬����Һ����������̼�ǵ���� | |
| B�� | ��ͬ��Ԫ����ɵ�����һ���Ǵ����� | |
| C�� | ��C��ʯī���TC�����ʯ������H=+1.90kJ•mol-1��֪��ʯī�Ƚ��ʯ�ȶ� | |
| D�� | ��101kPaʱ��2g H2��ȫȼ������Һ̬ˮ���ų�285.8 kJ���������ʾ����ȼ�յ��Ȼ�ѧ����ʽΪ��2H2��g��+O2 ��g���T2H2O��l������H=-285.8kJ•mol-1 |
| A�� | ����һ����������ƽ��Ŀ��淴Ӧ�����ӷ�Ӧ������ʵ���������Ӧ����һ������ | |
| B�� | �ı��������ʹ��ѧ��Ӧ���ʷ����ı䣬��ѧƽ��һ�������ƶ� | |
| C�� | �����ܸı����Ӱٷ���������һ�����Ըı仯ѧ��Ӧ���ʺͻ�ѧƽ�� | |
| D�� | �����¶ȣ������淴Ӧ���ʾ�����ƽ�������ȷ�Ӧ�����ƶ� |
| A�� | �٢� | B�� | �ۢ� | C�� | �٢ڢۢ� | D�� | �٢ڢۢܢ� |
| A�� | ��˳�緽��ĵ��ݴ��� | |
| B�� | �ý��д���Һ��ë����ס�ڱ�Ѹ������ | |
| C�� | ����緽��ĸߴ��� | |
| D�� | ����������Ŀ��ý�ʪ���ޱ��º��Ŵ�������ʱ�����Ԯ |
| A�� | ���ʵ���Ũ��Ϊ0.5mol/L��MgCl2��Һ�У�����Cl-����ΪNA | |
| B�� | ͨ��״���£�NA��CO2����ռ�е����Ϊ22.4 L | |
| C�� | ���³�ѹ�£�1.06g Na2CO3���е�Na+��Ϊ0.02 NA | |
| D�� | ��״���£�22.4L �Ҵ����еķ�����ΪNA |

 ��
�� ��
�� ��������2-��-2-������
��������2-��-2-������