题目内容
【题目】现有下列9种微粒:![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 。按要求完成以下各题:
。按要求完成以下各题:
(1)![]() 、
、![]() 分别是氢元素的一种______,它们互为______。
分别是氢元素的一种______,它们互为______。
(2)互为同素异形体的微粒是______。
(3)![]() 的中子数为______,核外电子数为______。
的中子数为______,核外电子数为______。
(4)形成上述9种微粒的核素有______种、元素有______种。
【答案】核素 同位素 ![]() 和
和![]() 30 24 7 5
30 24 7 5
【解析】
根据核素、同位素、同素异形体和元素的概念结合核素的表示形式和质量数=质子数+中子数分析解答。
(1)![]() 、
、![]() 的质子数均为1、中子数分别为0、1,分别是氢元素的一种核素,它们互为同位素,故答案为:核素;同位素;
的质子数均为1、中子数分别为0、1,分别是氢元素的一种核素,它们互为同位素,故答案为:核素;同位素;
(2)同素异形体是同种元素组成的不同单质,![]() 、
、![]() 是氧元素组成的不同单质,互为同素异形体,故答案为:
是氧元素组成的不同单质,互为同素异形体,故答案为:![]() 和
和![]() ;
;
(3)![]() 的中子数=56-26=30,
的中子数=56-26=30,![]() 是铁原子失去2个电子形成,核外电子数=26-2=24,故答案为:30;24;
是铁原子失去2个电子形成,核外电子数=26-2=24,故答案为:30;24;
(4)9种微粒:![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 中,有7中核素
中,有7中核素![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() ,5种元素:H、C、N、Fe、O,故答案为:7;5。
,5种元素:H、C、N、Fe、O,故答案为:7;5。

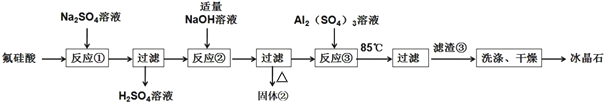
【题目】硫元素是动植物生长不可缺少的元素,广泛存在于自然界中。

从图1中选择符合图2要求的 X 、Y 代表的物质:X ______、Y ________。
(2)硫酸是重要的化工原料,小组同学对硫酸的工业制备和性质进行探究。查阅资料,工业制硫酸的过程如下:

①上述工业制硫酸过程中,没有发生氧化还原反应的过程是______________ 。(填“I ”“ II”或“III” )
②黄铁矿( FeS2 ) 中S为- 1价,完成过程 I 的化学反应方程式:______FeS2十______=_____Fe2O3+ _____SO2↑
③过程 II 中,小组同学在 500°C 和 10l kPa 条件下,将一定量的 SO2 和 O2充入含有催化剂的密闭容器中发生反应,随着反应的进行,用气体传感器测量各组分的浓度见下表
反应时间/ s | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 100 |
c ( SO2 ) / ( mol L -1) | 10 | 7 | 5 | 3.5 | 2 | 1 | 1 | 1 | 1 |
c ( O2 ) / ( mol L -1) | 5 | 3.5 | a | 1.75 | 1 | 0.5 | b | 0.5 | 0.5 |
c ( SO3 ) / ( mol L -1) | 0 | 3 | 5 | 6.5 | 8 | 9 | 9 | 9 | 9 |
数据分析,表中 a 、b 代表的数值分别是:a =________、b = _______;小 组同学判断 SO2 和 O2的 反应 50 秒后处于平衡状态,他们的判断依据是___________。
(3)浓硫酸与木炭在加热条件下可发生化学反应 ,为了检验反应产物,某同学设计了如下图所示的实验(部分夹持装置省略)。回答相关问题

①浓硫酸与木炭反应的化学方程式是 ________________。
②装置 A 中的实验现象是____________;证明的产物是___________ 。
③装置 C 的作用是_______________ 。
④该同学认为,如果去掉装置 B 也能实现产物的验证,该同学依据的实验现象及推理过程是__________________。