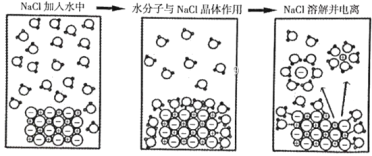
��Ŀ����
����Ŀ��ijС��ͬѧ�Բ�ͬ����̽��Cu����FeCl3��Һ�ķ�Ӧ��
��1����ͬѧ��FeCl3��Һ�м���Cu�ۣ��۲쵽��Һ����ɫ��Ϊdz��ɫ���ɴ�֤�������˷�Ӧ�������ӷ���ʽ��__��
��2����ͬѧͨ����Ӧ�������֤����������Ӧ�ķ�������Cu�ۼ��뵽��������KSCN��FeCl3��Һ�У��۲쵽��Һ��ɫ��ɫ���а�ɫ����A������
���ɫ����A���������ϣ�A����ΪCuCl��CuSCN��������Ԫ�صĻ��ϼ�Ϊ-2�ۣ��е�һ�ֻ����֡�ʵ��������£�
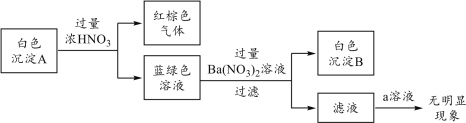
��ش�
�ٸ��ݰ�ɫ����B��__���ѧʽ�����жϳ���A��һ������CuSCN��
�ڽ����ݰ�ɫ����A�����ŨHNO3��Ӧ������ʵ���������жϰ�ɫ����A��һ������CuSCN����������ԭ�Ƕ�˵�����ɣ�__��
������Һ�м���a��Һ������������˵��A����CuCl����a��__���ѧʽ����
��������ʵ�飬֤��A��ΪCuSCN��
�ܽ�һ���������ϲ�ʵ����֤��CuSCN�ij����÷�Ӧ�ķ���ʽ����������
_Cu2+��_SCN-=_CuSCN����_(SCN)2
�ݽ�����������Լ�Fe(SCN)3![]() Fe3+��3SCN-��ƽ�⣬������2������Һ��ɫ��ȥ��ԭ��__��
Fe3+��3SCN-��ƽ�⣬������2������Һ��ɫ��ȥ��ԭ��__��
��3����֪(SCN)2��Ϊ��±�أ�����������Br2�������KSCN��Һ���루1�����õ���Һ�У��۲쵽��Һ���ɫ������Һ���Ŀ���ԭ����__��__��
���𰸡�2Fe3++Cu=2Fe2++Cu2+ BaSO4 +1��ͭҲ���Խ�Ũ���ỹԭ AgNO3 2 4 2 1 Cu��Fe3+��Ӧ����Cu2+ʹc(Fe3+)���٣�Cu2+��SCN-��Ӧ����CuSCN����ʹc(SCN-)���٣���ʹƽ��Fe(SCN)3![]() Fe3+��3SCN-�����ƶ�������Fe(SCN)3Ũ�ȼ�С����Һ��ɫ��ȥ Fe3+��ʣ�� (SCN)2��Fe2+�����������е�������Fe2+����
Fe3+��3SCN-�����ƶ�������Fe(SCN)3Ũ�ȼ�С����Һ��ɫ��ȥ Fe3+��ʣ�� (SCN)2��Fe2+�����������е�������Fe2+����
��������
����һ���濼����Fe2+��Fe3+�����ʣ�һ����Ҳͨ���������̽��ʵ�����ʽ������һЩ�������ӵļ��鷽������ȷ���������ʱ�����Ҫע���ų��������ʶԼ�������в�����ʵ������ĸ��š�
(1)Fe3+��������ǿ��Cu2+����˷����ķ�Ӧ�����ӷ���ʽ�ǣ�![]() ��
��
(2)��ͨ������ʵ�����̿�֪��������A�к���CuSCN���ھ���������Ũ���ᴦ����SԪ�ػ�ת��Ϊ![]() ����ˣ����ڼ���������ᱵ��Һ�����BaSO4��ɫ����������֤������A�к���CuSCN��
����ˣ����ڼ���������ᱵ��Һ�����BaSO4��ɫ����������֤������A�к���CuSCN��
��������A��ɽ�ΪCuCl����ô�ù���Ũ���ᴦ��ʱ��CuCl��+1�۵�CuҲ���Խ�Ũ���ỹԭ����������ɫ�Ļ�ԭ����NO2�����Խ�ͨ������ɫ����������˵��A��һ����CuSCN��
����Ҫ֤��A�в���CuCl��ֻ�����ʵ����֤��ɫ����A�ܽ�����Һ�в���Cl-����ˣ�a��Һ��AgNO3��Һ��
�������ָ��SCN-�е�SΪ-2�ۣ����Է���ʽ��S��Ӧ���̬������Cu��Ӧ���̬�½������Ը÷�Ӧ�ķ���ʽΪ��![]() ��
��
�ݷ���(2)����Һ��ɫ��ȥ��ԭ��ʱ��һ����Ҫ����Fe3+����ԭ���µ�Ũ���½�����һ����ҲҪ��������������CuSCN��ɫ����������Ҳ������SCN-�����������µ�Ũ���½�����˺�ɫ��ȥ��ԭ��Ϊ��Cu��Fe3+��Ӧ����Cu2+ʹc(Fe3+)���٣�Cu2+��SCN-��Ӧ����CuSCN����ʹc(SCN-)���٣���ʹƽ��![]() �����ƶ�������Fe(SCN)3Ũ�ȼ�С����Һ��ɫ��ȥ��
�����ƶ�������Fe(SCN)3Ũ�ȼ�С����Һ��ɫ��ȥ��
(3)�����ָ����±��(SCN)2��������Br2�ӽ��������±��(SCN)2Ҳ���Խ�Fe2+����������Fe2+��ԭ�Խ�ǿ��Ҳ���ױ����������������Һ���ɫ��ԭ������ǣ�(SCN)2��Fe2+����������е�������Fe2+������

����Ŀ������ʵ�鷽���ܴﵽʵ��Ŀ�ĵ����� ��
��� | A | B | C | D |
ʵ�鷽�� |
|
|
|
|
ʵ��Ŀ�� | ʵ�����Ʊ��������� | ���������ˮ | ��֤�����������������Ҵ���Һ�з�����ȥ��Ӧ��������ϩ | �ռ���ϩ����֤������ˮ�����ӳɷ�Ӧ |
A. A B. B C. C D. D
����Ŀ��AlN���Ͳ���Ӧ��ǰ���㷺�����Ʊ��������о���Ϊ�ȵ㡣
����������£�
���� | �۵�/�� | �е�/�� | ��N2��Ӧ�¶�/�� | ��Ӧ������ֽ��¶�/�� |
Al | 660 | 2467 | ��800 | AlN����2000 ����1400������ AlCl3������181������ |
Mg | 649 | 1090 | ��300 | Mg3N2����800 |
(1)AlN���Ʊ���
�� ��ѧ�����������
��.һ���¶��£���AlCl3�����NH3Ϊԭ���Ʊ�AlN����Ӧ�Ļ�ѧ����ʽ��____________________��
��.������Ӧ���˵��¶ȷ�Χ��______�棨����ĸ����
a.75~100 b.600~1100 c.2000~2300
�� ����ֱ�ӵ�������
Al��N2��ֱ�ӻ���ΪAlN���壬AlN�ܽ�Al��������Ӧ���Լ������С������¶ȣ���Al���о��Ȳ�������Mg�ۣ���ʹAl����ȫ��ת��ΪAlN���塣�ù��̷����ķ�Ӧ�У�__________________��_________��2Al + N2 ![]() 2AlN��
2AlN��
��̼�Ȼ�ԭ����
��Al2O3��C��ʯī����N2Ϊԭ�ϣ��ڸ������Ʊ�AlN��
��֪����. 2Al2O3(s) 4Al(g) + 3O2(g) H 1 =��3351 kJ��mol-1
��. 2C(ʯī��s) + O2(g) = 2CO(g) H 2 =��221 kJ��mol-1
��. 2Al(g) + N2(g) = 2AlN(s) H 3 =��318 kJ��mol-1
����ƽ���ƶ�ԭ��������Ӧ���Է�Ӧ���Ŀ���Ӱ�죺______________________________________��
(2)AlN�����ʡ�AlN��ĩ�ɷ���ˮ�⡣��ͬ�����£���ͬ������AlN��ĩˮ��ʱ��ҺpH�ı仯��ͼ��ʾ��
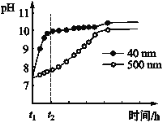
�� AlN��ĩˮ��Ļ�ѧ����ʽ��____________________________________��
�� ����t1-t2ʱ�����������߲���Ŀ���ԭ��_______________________________��
(3)AlN������⡣��a g AlN��Ʒ�м�������ŨNaOH��Һ��Ȼ��ͨ��ˮ������NH3ȫ����������NH3�ù�����v1 mL c1 mol��L-1 H2SO4��Һ������ȫ��ʣ���H2SO4��v2 mL c2 mol��L-1 NaOH��Һǡ���кͣ�����Ʒ��AlN������������________________________________��
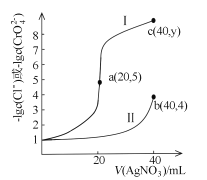
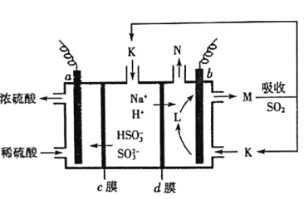
����Ŀ���������ա������ѭ�����ѳ������е�SO2���ɼ��ٶԴ�������Ⱦ�������£����ҺK������װ����ͼ��ʾ�����е��Һ��pH��![]() �仯�Ĺ�ϵ���±������жԴ��ж���ȷ����
�仯�Ĺ�ϵ���±������жԴ��ж���ȷ����
���Һ | n(SO32��)��n(HSO3��) | pH |
K | 9:91 | 6.2 |
L | 1:1 | 7.2 |
M | 91:9 | 8.2 |
A.�����Һ������ʱ��Һ�У�![]()
B.����ҺM����SO2����Ӧ�����ӷ���ʽΪ��![]()
C.HSO3����b�������ĵ缫��ӦʽΪ��![]()
D.��������״����2.24L����N����dĤ�Ϲ�ͨ��0.2mol������