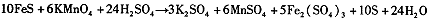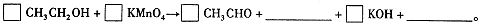��Ŀ����
Na2SO3�ڿ������ױ����������ʡ�ijͬѧΪ֤��Na2SO3�л�ԭ�ԣ���һƿʵ���ҳ��ڴ�ŵ�Na2SO3������ȡ����������ˮ������һ�������ռ���Һ��������ˮ������Һ��Ϊ��ɫ��
��1���ڼ�����Һ��Br2��Na2SO3��Ӧ�����ӷ���ʽ ��
��2����Ӧ�����Һ����SO32-��SO42-��Br-��OH-�������ӣ��±���ijͬѧ��������SO32-��SO42-��Br-��ʵ�鱨�棬�����δ����IJ��֡�
��ѡ�Լ���2 mol��L-1HCl��1 mol��L-1 H2SO4��l mol��L-1BaCl2��l mol��L-1Ba(NO3)2��1 mol��L-1 KMnO4��CCl4�����Ʊ�����ˮ��Ʒ����Һ��
| ��� | ʵ����� | Ԥ������ͽ��� |
| ����� | ȡ��������Һ�����Թ��У��������2mol��L-1HCl���ٵμ�����1 mol��L-1BaCl2 ��Һ�� | �а�ɫ�������ɣ�֤������Һ�к��С�SO42- �� |
| ����� | | |
| ����� | | |
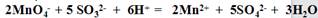
�ظ��������Σ�ÿ������0.10mol/LKMnO4��Һ����ֱ�Ϊ20.02 ml�� 20.00 ml��19.98 ml�������ԭ������Na 23 S 32 O 16)
�ټ�����Ʒ��Na2SO3����������Ϊ �����������3λ��Ч���֣�
�ڲ���ʱ����δ��0.10mol/L������KMnO4��Һ��ϴ�ζ��ܣ��ᵼ�²ⶨ��� �����ƫ�ߡ�����ƫ�͡���û��Ӱ�족��
33����1��SO32- + Br2 + 2 OH- = H2O + SO42- + 2Br- ��3�֣�δ��ƽ��1�֣�
��2����8�֣� ʵ����� Ԥ����������� ����� ����1��ȡ������������ϲ���Һ���Թ��У�����������ˮ���۲���Һ����ɫ����2�֣������ټ���CCl4�������ù۲���ɫҲ�ɣ� ��Һ�ʳȻ�ɫ��֤������Һ�к�Br-����2�֣����²�Һ��ʳȺ�ɫ��֤������Һ�к�Br-���� ����2����ȡ��������Һ���Թ��У�����������2 mol��L-1����ֱ������������Ϊֹ���ټ���������ˮ���۲���Һ����ɫ����2�֣������ټ������Ȼ�̼�������ú�۲���ɫҲ�ɣ� ��Һ�ʳȻ�ɫ��֤������Һ�к�Br-����2�֣����²�Һ��ʳȺ�ɫ��֤������Һ�к�Br-���� ����� ����1��ȡ��������������ϲ���Һ���Թ��У�����2��Ʒ�죬�۲���Һ����ɫ����2�֣� ��ɫ��ȥ�������SO32-����ɫ����ȥ������SO32-����2�֣� ����2����ȡ��������Һ���Թ��У��������2mol/L���ᣬ�ٵ���2��Ʒ��۲���Һ����ɫ����2�֣� ��ɫ��ȥ�������SO32-����ɫ����ȥ������SO32-����2�֣�
˵���������ֻ�����ᣬ�۲��������ݲ����������֡�
��3���� 0.630��63.0% ��3�֣�δע����Ч���ֿ�1�֣� �� ƫ����2�֣�.
�����������: ��1���ڼ�����Һ��Br2��Na2SO3����������ԭ��Ӧ�����ȶ������ӣ����������ᣬ�������ӷ���ʽΪ��SO32- + Br2 + 2 OH- = H2O + SO42- + 2Br- ��
��2��ʵ���Ŀ���Ǽ�����Һ�к��е�SO32-��SO42-��Br- �����Կ�����ѡ����Ӧ��ʵ�ʽ��м��顣SO42- ����ѡ��BaCl2 ��Һ������Ӧ��������������İ�ɫ���������֤��SO42- ����Br- ���飬���������䵥�����ױ��л��ܼ���ȡ����ɫ�����������Կ��Լ���ǿ������������ˮ���л��ܼ�CCl4 ������SO32- �н�ǿ��ԭ�ԣ��Һ�ǿ�ᷴӦ�����д̼�����ζ�����壬�ܹ�Ư��Ʒ����Һ�����Կ�������Ư���Խ��м��顣���Ծ��岽������� ʵ����� Ԥ����������� ����� ����1��ȡ������������ϲ���Һ���Թ��У�����������ˮ���۲���Һ����ɫ����2�֣������ټ���CCl4�������ù۲���ɫҲ�ɣ� ��Һ�ʳȻ�ɫ��֤������Һ�к�Br-����2�֣����²�Һ��ʳȺ�ɫ��֤������Һ�к�Br-���� ����2����ȡ��������Һ���Թ��У�����������2 mol��L-1����ֱ������������Ϊֹ���ټ���������ˮ���۲���Һ����ɫ����2�֣������ټ������Ȼ�̼�������ú�۲���ɫҲ�ɣ� ��Һ�ʳȻ�ɫ��֤������Һ�к�Br-����2�֣����²�Һ��ʳȺ�ɫ��֤������Һ�к�Br-���� ����� ����1��ȡ��������������ϲ���Һ���Թ��У�����2��Ʒ�죬�۲���Һ����ɫ����2�֣� ��ɫ��ȥ�������SO32-����ɫ����ȥ������SO32-����2�֣� ����2����ȡ��������Һ���Թ��У��������2mol/L���ᣬ�ٵ���2��Ʒ��۲���Һ����ɫ����2�֣� ��ɫ��ȥ�������SO32-����ɫ����ȥ������SO32-����2�֣�
��3������ʵ�����ݿɵã�ƽ��ÿ�εζ�����KMnO4 ��Һ���V=��20.02 ml+20.00 ml+19.98 ml����3="20.00" ml���ɷ���ʽ��֪�ζ���Ӧ��n(KMnO4 ): n(Na2SO3 )=2:5������n(Na2SO3 )="2.5" n(KMnO4 )="2.5��20.00" ml��10-3��0.10mol/L="0.005" mol��������Ʒ���ܵ�n(Na2SO3 )="10��0.005" mol=0.050mol������Na2SO3 ��Ʒ�Ĵ���=0.050mol��126g/mol��10.0g��100%=63.0%��
�ڸ���c��=c�ꡤV��/V���֪����δ��0.10mol/L������KMnO4��Һ��ϴ�ζ��ܣ����ʹ��ҺKMnO4��Ũ�ȼ�С��Ũ�ȼ�С������ĸ���ı�Һ������V�������´���Һ��Ũ��ƫ�ߡ�
���㣺���⿼�����ʵ��̽����������ԭ����ʽ��ƽ��������ԭ�ζ���

��10�֣�ij�о���ѧϰС��ͬѧ��Fe(NO3)3��Һ�еμӵ���KI��Һ����Һ����ɫ�����Ƕ�Fe(NO3)3��Һ�н�I������������������������̽����
��ʵ�顿�ֱ���FeCl3��Һ��HNO3��Һ�еμӵ���KI��Һ������Һ������ɫ��
��1��FeCl3��Һ��KI��Һ��Ӧ�����ӷ���ʽΪ ��
��2��KI��HNO3��Ӧ�����ӷ���ʽΪI����H����NO3����NO����I2��H2O(δ��ƽ)����Ӧ���������뻹ԭ�������ʵ���֮��Ϊ ��
��������衿����1��������ֻ��Fe3�� ����2��������ֻ��NO3����H����
�����ʵ�鷽������֤���衿
��3�������ʵ����֤��������
��ѡ�Լ���0.2mol?L��1��Fe(NO3)3��Һ��0.2mol?L��1��KI��Һ��0.01mol?L��1��KMnO4������Һ��0.01mol?L��1��KSCN��Һ��CCl4��Һ��������Һ������ʾ��NO3���ڲ�ͬ�����µĻ�ԭ����ϸ��ӣ���ʱ���Թ۲쵽���������
| ʵ�鲽�� | Ԥ������ͽ��� |
| ��ȡ5ml0.2mol?L��1��Fe(NO3)3��Һ��5ml0.2mol?L��1��KI��Һ����ַ�Ӧ�����5ml CCl4��Һ�����ã�ȡ�ϲ���Һ��������A��B��֧�Թ��� | |
| �� �� | ����Һ�����ɫ�������1�������������1�������� ����Һ����ɫ�������2�������������2������ |
�뵼�������г���Ҫ���Ʋ��ӣ��Ա�֤���Ƶ�����,���Ȼ���(PCl3)��һ����Ҫ�IJ��Ӽ���ʵ����Ҫ�û���(������)������Cl2ģ�ҵ������ȡPCl3,װ������ͼ��ʾ:�����ּг�װ����ȥ��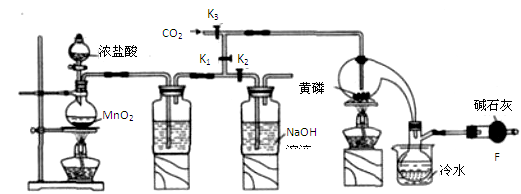
A B C D E
��֪����������Cl2��Ӧ����PCl3,�����Cl2��Ӧ����PCl5 PCl3��ˮ��ǿ��ˮ������ H3PO3��HC1����O2������POCl3,POCl3����PCl3,PCl3��POCl3���۷е���±���
| ���� | �۵�/�� | �е�/�� |
| PCl3 | -112 | 75.5 |
| POCl3 | 2 | 105.3 |
��ش��������⣺
��1��Aװ���������������ӷ���ʽΪ ��
��2��B����װ�Լ��� ,
E����ˮ��������
F�м�ʯ�ҵ�������_____
��3��ʵ��ʱ,���װ�������Ժ�,�ȴ�K3ͨ������CO2,��Ѹ�ټ�����ס�ͨ����CO2�������� ��
��4���ֲ�Ʒ�г�����POCl3��PCl5�ȡ���������ȳ�ȥPCl5��.ͨ��_____(��ʵ��������ƣ�,���ɵõ��ϴ�����PCl3��
��5��ͨ�����淽���ɲⶨ��Ʒ��PCl3����������
��Ѹ�ٳ�ȡ1.00g��Ʒ,��ˮ��Ӧ�����250 mL��Һ��
��ȡ������Һ25.00mL,�����м����ˮ,��ַ�Ӧ��
�����������Һ�м��뼸�ε�����Һ,��0.1000 mol/L��Na2S2O3,��Һ�ζ�
���ظ��ڡ��۲���,ƽ������Na2S2O3,��Һ8.40mL
��֪��H3PO3+H2O+I2="=" H3PO4+2HI��I2+2Na2S2O3==2NaI+Na2S4O6,����ⶨ������û��������Ӧ��������������,�ò�Ʒ��PC13����������Ϊ_______��
ij��ȤС�鼷��SO2���廹ԭFe3+��I2������ʹ�õ�ҩƷ��װ������ͼ��ʾ��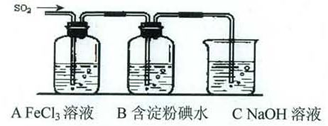
��1��SO2���廹ԭFe3+��Ӧ�IJ�����_____________��_____________�������ӷ��ţ���
��2������ʵ�鷽������������ʵ������ȡ����SO2����____��
| A��Na2SO3��Һ��HNO3 | B��Na2SO3������Ũ���� |
| C���������ڴ�����ȼ�� | D��ͭ����ŨH2SO4 |
��4�������280 mL SO2���壨������Ϊ��̬������Cװ���У���C��50 mL NaOH��Һ��Ũ������Ϊ_____________mol/L���ܴﵽĿ�ġ�
��5��������װ����ͨ�������SO2Ϊ����֤A��SO2��Fe3+������������ԭ��Ӧ������ȡA�е���Һ���ֳ����ݣ������������ʵ�飺
�����٣�����һ����Һ�м���KMnO4��Һ���Ϻ�ɫ��ȥ��
�����ڣ�����һ����Һ����KSCN��Һ������죬�ټ������Ƶ���ˮ����Һ��졣
�����ۣ����ڶ�����Һ������ϡ�����ữ��BaCl2��������ɫ������
������������������____��ԭ����_______________________________________��
��6���ܱ���I-�Ļ�ԭ������SO2��������_________________________________________��д���й����ӷ���ʽ��_______________________________________��
ij��ѧС����ѧϰԪ�������ɺԽ̲���Fe2+����ΪFe3+��ʵ���һ��˼������������⣺Cl2�ܽ�Fe2+����ΪFe3+����ôBr2��I2�ܷ�Fe2+����ΪFe3+��
����һ�������Ʋ�
����ͬѧ��ΪBr2��I2�����ܽ�Fe2+����ΪFe3+������˼���������� ��
����ͬѧ��ΪBr2��I2�����ܽ�Fe2+����ΪFe3+������ͬѧ��ΪBr2�ܽ�Fe2+����ΪFe3+��I2���ܡ�����˼���������Ǵ��ϵ���±�ص��������Լ�����
���ڶ������ʵ�������֤
�ڴ��Թ��м��������ۣ�����10 mL ϡ���ᣬ���Թܣ���ַ�Ӧ��������ʣ�࣬ȡ�ϲ���Һ��������ʵ�顣
ʵ��1��
| �Թ� | ���� | ���� |
| �� | �����Թ��м���2 mL FeCl2��Һ���ٵμ���������ɫ����ˮ�����Թ� | ��ҺΪ��ɫ |
| �� | �����Թ��м���2 mL FeCl2��Һ���ٵμ������ػ�ɫ�ĵ�ˮ�����Թ� | ��ҺΪ��ɫ |
��������ʵ������ķ��������
��1��ͬѧ����Ϊ��������˵����ˮ�ܽ�Fe2+���������ӷ���ʽΪ ��
ͬѧ����ΪӦ�ò���ʵ�飬���ܵó�ͬѧ�Ľ��ۡ��������ͬѧ�����ʵ�飺
ʵ��2��
| ���� | Ӧ�ù۲쵽������ |
| | |
��2����С��ͬѧ�Ԣ�����Һ�ʻ�ɫ��ԭ��չ�������ۣ�
����1����ˮ��FeCl2��Һ����Ӧ����ɫ�ǵ�ˮϡ�ͺ����ɫ��
����2�� ��
ʵ��3������ʵ����ȷ�����ܵ�ԭ��
| ���� | ���� |
| ���Թܢ�������Һ�м�������0.5 mLCCl4�����������һ��ʱ���ȡ���ϲ���Һ���μ�KSCN ��Һ | ���ú��ϲ���Һ������ɫ���²���ҺΪ��ɫ���ϲ���Һ�μ�KSCN ��Һ����dz��ɫ |
ͬѧ����Ϊ��ʵ���������˵���ǡ�����2��������ͬѧ����Ϊ���Ͻ������������ʵ��4��
ʵ��4��
| ���� | ���� |
| ����һ֧�Թ��м���2 mL FeCl2��Һ���μ�0.5mL��ˮ���ټ���0.5mL �������������������һ��ʱ���ȡ���²���Һ���μ�KSCN ��Һ | ���ú��ϲ�ҺΪ��ɫ���²�Һ������ɫ���²���Һ�μ�KSCN��Һ��û�г���dz��ɫ |
����Ϊʵ��4��Ƶ���ҪĿ���� ��
ͬѧ������ʵ��4����ó����ۣ��ڱ���ʵ�������£���ˮ��FeCl2��Һ��Ӧ�ij̶Ⱥ�С��
��3��Cl2��Br2��I2����Fe2+��������������ԭ�ӽṹ����ԭ�� ��
���н����У�������Ȼ�γɵ��������ܱ����ڲ��������������������
| A��K | B��Na | C��Fe | D��Al |
���Ƶ�˼ά�����ǻ�ѧѧϰ���о��г��õ���Ҫ˼ά�����������ý���Ҫ����ʵ���ļ������ȷ������ȷ������������յ�֪ʶ���ж��������ƽ�������ȷ����
| | ��ѧ��ʵ | ���ƽ��� |
| A | pH��3������ϡ��1000����pH��6 | pH��6������ϡ��1000����pH��9 |
| B | �õ������MgCl2�ķ���ұ������þ | �õ������NaCl�ķ���ұ�������� |
| C | ��SO2ͨ��BaCl2��Һ���������� | ��SO2ͨ��Ba(NO3)2��Һ��Ҳ�������� |
| D | Al��O2��ȼ������Al2O3 | Fe��O2��ȼ������Fe2O3 |
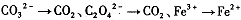 ���ҳ�����һ���仯�롰
���ҳ�����һ���仯�롰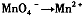 �����һ����Ӧ��д���÷�Ӧ�����ӷ���ʽ____ ��
�����һ����Ӧ��д���÷�Ӧ�����ӷ���ʽ____ ��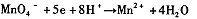
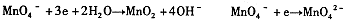 �ɴ˿�֪������������ӣ�MnO��4����Ӧ��IJ����� �йء�
�ɴ˿�֪������������ӣ�MnO��4����Ӧ��IJ����� �йء�