题目内容
【题目】有以下物质:①石墨;②氯化氢气体;③酒精;④氨水;⑤二氧化碳;⑥碳酸氢钠固体;⑦氯化铁溶液;⑧纯醋酸;⑨氧化钠固体;⑩铝。
(1)属于非电解质的是______________;属于强电解质的是__________;属于弱电解质的是___________。(用序号填空)
(2)写出物质⑥溶于水溶液显碱性的原因_______(用离子方程式和简要文字说明作答)
(3)写出物质⑥和⑧在水中反应的离子方程式:_____________。
(4)配制溶液⑦时通常将⑦先溶于___________,然后再加水稀释,通过增加溶液中_______的浓度以防止其发生水解。
(5)浓度、体积相同的②和⑧的溶液,加入相同形状且足量的Zn粒,反应速率快的是___(用序号填空);pH值、体积相同的②和⑧的溶液时,产生气体的量多的是________。(用序号填空)
【答案】③⑤ ②⑥⑨ ⑧ 因发生HCO3-![]() H++CO32—和HCO3- + H2O
H++CO32—和HCO3- + H2O![]() H2CO3 + OH—,其中HCO3-的水解程度大于其电离程度,使溶液中c(OH-)> c(H+) HCO3-+CH3COOHCH3COO-+CO2↑+H2O 浓盐酸 H+ ② ⑧
H2CO3 + OH—,其中HCO3-的水解程度大于其电离程度,使溶液中c(OH-)> c(H+) HCO3-+CH3COOHCH3COO-+CO2↑+H2O 浓盐酸 H+ ② ⑧
【解析】
(1)非电解质是在水溶液中或熔融状态下都不能能够导电的化合物;强电解质是在水溶液中或熔融状态下能完全电离的电解质;弱电解质是在水溶液中不能完全电离的电解质;
(2)碳酸氢钠溶液中,碳酸氢根的水解程度大于电离程度,使溶液中c(OH-)> c(H+);
(3)由醋酸的酸性强于碳酸的酸性可知,醋酸与碳酸氢钠溶液反应生成醋酸钠、二氧化碳和水;
(4)氯化铁溶液中三价铁离子在溶液中水解使溶液呈酸性,配制氯化铁溶液时,应增加溶液中氢离子浓度拟制氯化铁水解;
(5)因盐酸是强酸,醋酸是弱酸,浓度、体积相同的盐酸和醋酸溶液中,盐酸溶液中氢离子浓度大于醋酸;pH值、体积相同的盐酸和醋酸溶液中,醋酸浓度大于盐酸。
(1)非电解质是在水溶液中或熔融状态下都不能能够导电的化合物,③酒精和⑤二氧化碳都是非电解质;强电解质是在水溶液中或熔融状态下能完全电离的电解质,包括强酸、强碱、活泼金属氧化物和大部分盐,②氯化氢气体、⑥碳酸氢钠固体、⑨氧化钠固体都是强电解质;弱电解质是在水溶液中不能完全电离的电解质,包括弱酸、弱碱、水等,⑧纯醋酸是弱电解质,故答案为:③⑤;⑥⑨;⑧;
(2)碳酸氢钠溶液中,碳酸氢根离子即存在电离趋势:HCO3-![]() H++CO32—,也存在水解趋势:HCO3- + H2O
H++CO32—,也存在水解趋势:HCO3- + H2O![]() H2CO3 + OH—,因溶液中碳酸氢根的水解程度大于电离程度,使溶液中c(OH-)> c(H+),溶液呈碱性,故答案为:因发生HCO3-
H2CO3 + OH—,因溶液中碳酸氢根的水解程度大于电离程度,使溶液中c(OH-)> c(H+),溶液呈碱性,故答案为:因发生HCO3-![]() H++CO32—和HCO3- + H2O
H++CO32—和HCO3- + H2O![]() H2CO3 + OH—,其中HCO3-的水解程度大于其电离程度,使溶液中c(OH-)> c(H+);
H2CO3 + OH—,其中HCO3-的水解程度大于其电离程度,使溶液中c(OH-)> c(H+);
(3)由醋酸的酸性强于碳酸的酸性可知,醋酸与碳酸氢钠溶液反应生成醋酸钠、二氧化碳和水,反应的离子方程式为HCO3-+CH3COOH=CH3COO-+CO2↑+H2O,故答案为:HCO3-+CH3COOH=CH3COO-+CO2↑+H2O;
(4)氯化铁溶液中三价铁离子在溶液中水解使溶液呈酸性,配制氯化铁溶液时,通常将氯化铁先溶于浓盐酸,然后再加水稀释,通过增加溶液中氢离子浓度的方法防止氯化铁水解,故答案为:浓盐酸;H+;
(5)因盐酸是强酸,醋酸是弱酸,浓度、体积相同的盐酸和醋酸溶液中,盐酸溶液中氢离子浓度大于醋酸,则与相同形状且足量的Zn粒反应时,盐酸的反应速率快于醋酸;pH值、体积相同的盐酸和醋酸溶液中,醋酸浓度大于盐酸,则与相同形状且足量的Zn粒反应时,醋酸生成氢气的物质的量大,故答案为:②;⑧。

 阅读快车系列答案
阅读快车系列答案【题目】汽车尾气污染是由汽车排放的废气造成的环境污染。主要污染物为一氧化碳、碳氢化合物、氮氧化合物等,对人类和动、植物危害甚大。解决汽车尾气问题的主要方法是研究高效催化剂促使尾气中的一氧化碳和氮氧化物反应,转化成无污染的氮气和二氧化碳。
回答下列问题:
(1)在Co+的催化作用下,CO(g)还原N2O(g)的反应历程和能量变化如图所示(逸出后物质认为状态下发生变化,在图中略去)。已知总反应的化学方程式为:CO(g)+N2O(g)![]() CO2(g)+N2(g)。
CO2(g)+N2(g)。
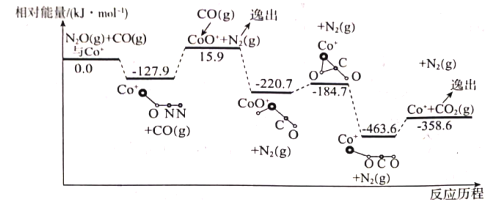
该反应分两步进行:
第一步:Co+(s)+N2O(g)![]() CoO+(s)+N2(g) △H1=+15.9kJmol-1;
CoO+(s)+N2(g) △H1=+15.9kJmol-1;
笫二步:___;△H2=___;
①填写第二步反应的热化学方程式,并根据反应历程图计算△H2的数值。
②该反应的最高能垒(活化能)为___。
(2)500℃条件下,在容积均为2L的三个密闭容器中,按不同方式投入反应物,发生上述反应,测得相关数据如下表:
容器 | 反应物投入的量 | 平衡时 n(N2/mol) | 达到平衡所需时间/min | 平衡时能量变化/kJ |
甲 | 1molCO和1molN2O | n1 | t1 | 放热Q1 |
乙 | 2molCO和2molN2O | n2 | t2 | 放热Q2 |
丙 | 2molCO2和2molN2 | n3 | t3 | 吸热Q3 |
①Q1+![]() ___358.6(填“>”“=”或“<”下同,t1___t2;
___358.6(填“>”“=”或“<”下同,t1___t2;
②500℃条件下,乙和丙两容器,气体混合物中N2O的物质的量分数x(N2O)与反应时间t的关系如下表:
t/s | 0 | 20 | 40 | 60 | 80 | 120 | |
乙 | x(N2O) | 0.5 | 0.32 | 0.20 | 0.12 | 0.088 | 0.07 |
丙 | x(N2O) | 0 | 0.030 | 0.048 | 0.059 | 0.065 | 0.07 |
根据上述实验结果,计算出乙容器中0~20s时间内的化学反应速率v(CO)=___;该反应的平衡常数K数值为:___;(保留3位有效数字)
③请推测并在图中画出甲容器中x(N2O)随时间变化的关系图象,标出恰好达到平衡时刻点的位置___。

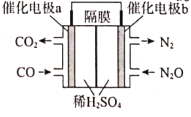
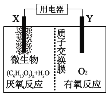
(3)若将CO(g)还原N2O(g)的反应设计成如图的原电池装置,则该电池正极的电极反应式为___。