题目内容
【题目】对于氨气的催化氧化反应:4NH3 +5O2 =4NO + 6H2O
(1)该反应中的还原剂是________,被还原的元素是_________ ;
(2)用单线桥标出该反应中电子转移的方向和数目;4NH3 +5O2 =4NO + 6H2O_________
(3)若反应转移了2mol电子,则产生的气体在标准状态下体积约为_______。
【答案】NH3(氨气) O(氧或氧元素) 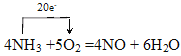 8. 96L
8. 96L
【解析】
在反应4NH3 +5O2 =4NO + 6H2O中,NH3 中的N元素由-3价升高到+2价,O2中的O元素由0价降低到-2价。
(1)该反应中,还原剂是含有化合价降低元素的反应物,被还原的元素是反应物中化合价降低的元素;
(2)用单线桥标出该反应中的电子转移方向,是从反应物中化合价升高元素指向化合价降低元素,数目是得电子总数或失电子总数;
(3)确定本反应的电子转移数目,然后建立NO与电子转移数目关系式,利用反应转移的2mol电子,算出生成NO的物质的量,从而算出其在标准状态下体积。
(1)该反应中,还原剂是含有化合价降低元素的反应物,则还原剂是NH3(氨气),被还原的元素是反应物中化合价降低的O(氧或氧元素)素;答案为:NH3(氨气);O(氧或氧元素);
(2)用单线桥标出该反应中的电子转移和数目为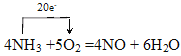 ;答案为:
;答案为: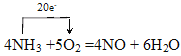 ;
;
(3)由单线桥表示的电子转移方向和数目的反应,可得出如下关系式:NO——5e-,现反应中转移2mol电子,则n(NO)=![]() =0.4mol,V(NO)=0.4mol×22.4L/mol=8. 96L。答案为:8. 96L。
=0.4mol,V(NO)=0.4mol×22.4L/mol=8. 96L。答案为:8. 96L。

 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案【题目】某化学实验小组用酸性KMnO4溶液和草酸(H2C2O4)溶液反应,研究外界条件反应速率的影响,实验操作及现象如下:
编号 | 实验操作 | 实验现象 |
I | 向一支试管中先加入1mL 0.01 mol/L酸性 KMnO4溶液,再加入1滴3mol/L硫酸和9滴蒸馏水,最后加入1mL 0.1mol/L草酸溶液 | 前10min内溶液紫色无明显变化,后颜色逐渐变浅, 30 in后几乎变为无色 |
II | 向另一支试管中先加入1mL 0.01mol/L酸性 KMnO4溶液,再加入10滴3mol/L硫酸,最后加入1mL 0.1mol/L草酸溶液 | 80s内溶液紫色无明显变化,后颜色迅速变浅,约150s后几乎变为无色 |
(1)高锰酸钾与草酸反应的离子方程式:______________________________________
(2)由实验I、II可得出的结论是____________________________。
(3)关于实验II中80s后溶液颜色迅速变浅的原因,该小组提出了猜想:该反应中生成的Mn2+对反应有催化作用。利用提供的试剂设计实验III,验证猜想。
提供的试剂:0.01mol/L酸性 KMnO4溶液,0.1mol/L草酸溶液,3mol/L硫酸,MnSO4溶液,MnSO4固体,蒸馏水
① 补全实验III的操作:向试管中先加入1mL 0.01mol/L酸性 KMnO4溶液,______,最后加入1mL 0.1mol/L草酸溶液。
② 若猜想成立,应观察到的实验现象是______。
(4)该小组拟采用如图所示的实验方案继续探究外界条件对反应速率的影响。

① 他们拟研究的影响因素是______。
② 你认为他们的实验方案______(填“合理”或“不合理”),理由是______。