题目内容
【题目】NA为阿伏加德罗常数的值。下列说法正确的是( )
A.标准状况下,2.24LCH3OH分子中共价键的数目为0.5NA
B.100g46%的甲酸(HCOOH)水溶液中所含的氧原子数目为5NA
C.lmol铁粉高温下与足量水蒸气反应,转移电子数为3NA
D.2molSO2和lmolO2在催化剂作用下充分反应所得分子总数为2NA
【答案】B
【解析】
A.标准状况下CH3OH为液体,不能用n=V/Vm进行计算其物质的量,A选项错误;
B.100g46%的甲酸(HCOOH)水溶液中甲酸的物质的量为![]() ,则H2O的质量为100-46g=54g,物质的量为
,则H2O的质量为100-46g=54g,物质的量为![]() ,1mol甲酸中含有的氧原子为2mol,3molH2O含有3mol氧原子,总共含有2+3=5mol氧原子,个数为5NA,B选项正确;
,1mol甲酸中含有的氧原子为2mol,3molH2O含有3mol氧原子,总共含有2+3=5mol氧原子,个数为5NA,B选项正确;
C.lmol铁粉高温下与足量水蒸气反应,反应方程式为3Fe+4H2O(g)![]() Fe3O4+4H2,反应中Fe的化合价由0价升高至+2、+3价,3molFe转移8mol电子,则1mol转移
Fe3O4+4H2,反应中Fe的化合价由0价升高至+2、+3价,3molFe转移8mol电子,则1mol转移![]() 电子,个数为
电子,个数为![]() ,C选项错误;
,C选项错误;
D.SO2和O2在催化剂作用下反应的化学方程式为2SO2+O2![]() 2SO3,反应为可逆反应,不能进行到底,则2molSO2和lmolO2在催化剂作用下充分反应所得分子总数大于2NA,D选项错误;
2SO3,反应为可逆反应,不能进行到底,则2molSO2和lmolO2在催化剂作用下充分反应所得分子总数大于2NA,D选项错误;
答案选B。

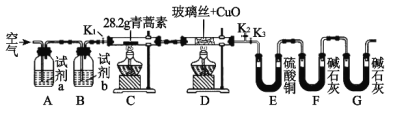
【题目】青蒿素是一种高效的抗疟药,某研究性学习小组的同学通过查阅资料获得如下信息:青蒿素是由碳、氢、氧三种元素所组成的,熔点为156~157℃,他们设计了如下装置来测量青蒿素的分子组成,回答下列问题:
装置 | 实验前/g | 实验后/g |
E | 22.6 | 42.4 |
F | 80.2 | 146.2 |
(1)试剂加入后首先要进行的操作是_____________,其目的是____________,实验中需要对开关K1、K2、K3进行操作,首次对开关K1、K2、K3进行操作的方法是________,适当时间后再关闭相应的开关,为提高实验的准确性,在C处停止加热后还应进行的操作是____________。
(2)试剂a、b分别是________________________________________,点燃C、D处酒精灯的先后顺序是___________________________,使用装置D的目的是___________。
(3)E中使用硫酸铜相对于使用CaCl2的好处(不考虑吸收效果的差异性)是_____。
(4)充分反应后获得的有关数据如上表(假设生成的气体全部被吸收):则测得青蒿素的最简式是_________________________。
(5)若要求出青蒿素的分子式,还需要通过实验测量出一个数据,请你指出该数据是什么,测量出该数据的方法是(只考虑理论上的可能性):___________。