题目内容
13.Ⅰ.写出下列有机物的系统命名或结构简式:(1)
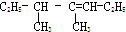 4,5-二甲基-3-庚烯
4,5-二甲基-3-庚烯(2)
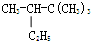 2,2,3一三甲基戊烷
2,2,3一三甲基戊烷(3)2,5-二甲基-4-乙基庚烷(CH3)2CHCH2CH(C2H5)CH(CH3)CH2CH3.
分析 判断有机物的命名是否正确或对有机物进行命名,其核心是准确理解命名规范:
(1)烷烃命名原则:
①长:选最长碳链为主链;
②多:遇等长碳链时,支链最多为主链;
③近:离支链最近一端编号;
④小:支链编号之和最小.看下面结构简式,从右端或左端看,均符合“近-----离支链最近一端编号”的原则;
⑤简:两取代基距离主链两端等距离时,从简单取代基开始编号.如取代基不同,就把简单的写在前面,复杂的写在后面;
(2)有机物的名称书写要规范;
(3)对于结构中含有苯环的,命名时可以依次编号命名,也可以根据其相对位置,用“邻”、“间”、“对”进行命名;
(4)含有官能团的有机物命名时,要选含官能团的最长碳链作为主链,官能团的位次最小;
根据有机物的命名原则对有机物命名、根据有机物名称结合命名原则写成有机物的结构简式.
解答 解:(1)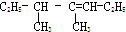 分子中最长碳链含有7个C,7编号从右端开始,该有机物名称为:4,5-二甲基-3-庚烯,故答案为:4,5-二甲基-3-庚烯;
分子中最长碳链含有7个C,7编号从右端开始,该有机物名称为:4,5-二甲基-3-庚烯,故答案为:4,5-二甲基-3-庚烯;
(2)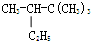 分子中最长碳链含有5个C,该有机物名称为:2,2,3一三甲基戊烷,故答案为:2,2,3一三甲基戊烷;
分子中最长碳链含有5个C,该有机物名称为:2,2,3一三甲基戊烷,故答案为:2,2,3一三甲基戊烷;
(3)2,5-二甲基-4-乙基庚烷,最长的主链含有7个C原子,甲基处于2、5号碳原子上,乙基处于4号碳原子上,其结构简式为:CH3)2CHCH2CH(C2H5)CH(CH3)CH2CH3,故答案为:(CH3)2CHCH2CH(C2H5)CH(CH3)CH2CH3.
点评 本题考查了有机物的系统命名法,题目难度中等,该知识点是高考考查的重点和难点,解答本题的关键是熟练掌握常见有机物的命名规则,试题有利于培养学生灵活应用所学知识的能力.

练习册系列答案
相关题目
3.下列关于镁的说法中,不正确的是( )
| A. | 镁是一种银白色固体 | |
| B. | 镁是热和电的良导体 | |
| C. | 镁在自然界中主要以单质的形式存在 | |
| D. | 镁常温下能与氧气反应,生成一层致密的氧化薄膜 |
4.2015年8月12日23:30左右,天津滨海新区的一处集装箱码头发生爆炸,发生爆炸的是集装箱内的易燃易爆物品氰化钠,数量为700吨左右.
资料:氰化钠化学式为NaCN,白色结晶颗粒或粉末,易潮解,有微弱的苦杏仁气味.剧毒,皮肤伤口接触、吸入、吞食微量可中毒死亡.熔点563.7℃,沸点1496℃.易溶于水,易水解生成氰化氢,水溶液呈强碱性,是一种重要的化工原料,用于电镀、冶金和有机合成医药、农药及金属处理方面.
(1)用离子方程式表示其水溶液呈强碱性的原因:CN-+H2O?HCN+OH-.
(2)氰化钠要用双氧水或硫代硫酸钠中和.
①用双氧水处理产生一种酸式盐和一种能使湿润的红色石蕊试纸变蓝的气体,请写出该反应的化学方程式NaCN+H2O2+H2O=NaHCO3+NH3↑;
②用硫代硫酸钠中和的离子方程式为CN-+S2O32-→A+SO32-,A为SCN-(填化学式).
(3)含氰废水中的CN-有剧毒.
①CN-中C元素显+2价,N元素显-3价,则非金属性N>C(填<,=或>)
②在微生物的作用下,CN-能够被氧气氧化成HCO3-,同时生成NH3,该反应的离子方程式为2CN-+4H2O+O2$\frac{\underline{\;微生物\;}}{\;}$2HCO3-+2NH3.
(4)K2FeO4能非常充分的去除救援产生的废水(以下简称救援废水)中的CN-离子.根据K2FeO4加入的量,分别发生下列反应:
Ⅰ.3CN-+2FeO42-+5H2O¾→2Fe(OH)3+3CNO-+4OH-
Ⅱ.6CN-+10FeO42-+22H2O¾→10Fe(OH)3+6CO32-+3N2+14OH-
Ⅲ.3CN-+8FeO42-+17H2O¾→8Fe(OH)3+3CO32-+3NO2-+10OH-
Ⅳ.3CN-+10FeO42-+22H2O¾→10Fe(OH)3+3CO32-+3NO3-+14OH-
现取含CN-离子的救援废水,加入一定量的K2FeO4,控制溶液pH=11.2,反应10min后,CN-离子的去除率超过99%.(假定K2FeO4只与CN-反应)
实验①中,CN-被FeO42-氧化生成CNO-.
(5)室温下,0.1mol/L的氯化铵溶液和0.1mol/L的硫酸氢铵溶液,酸性更强的是NH4HSO4,
其原因是HSO4-有较大程度的电离,使溶液呈较强酸性.而NH4Cl只是NH4+水解呈弱酸性.已知:H2SO4:Ki2=1.2×10-2NH3•H2O:Ki=1.8×10-5.
资料:氰化钠化学式为NaCN,白色结晶颗粒或粉末,易潮解,有微弱的苦杏仁气味.剧毒,皮肤伤口接触、吸入、吞食微量可中毒死亡.熔点563.7℃,沸点1496℃.易溶于水,易水解生成氰化氢,水溶液呈强碱性,是一种重要的化工原料,用于电镀、冶金和有机合成医药、农药及金属处理方面.
(1)用离子方程式表示其水溶液呈强碱性的原因:CN-+H2O?HCN+OH-.
(2)氰化钠要用双氧水或硫代硫酸钠中和.
①用双氧水处理产生一种酸式盐和一种能使湿润的红色石蕊试纸变蓝的气体,请写出该反应的化学方程式NaCN+H2O2+H2O=NaHCO3+NH3↑;
②用硫代硫酸钠中和的离子方程式为CN-+S2O32-→A+SO32-,A为SCN-(填化学式).
(3)含氰废水中的CN-有剧毒.
①CN-中C元素显+2价,N元素显-3价,则非金属性N>C(填<,=或>)
②在微生物的作用下,CN-能够被氧气氧化成HCO3-,同时生成NH3,该反应的离子方程式为2CN-+4H2O+O2$\frac{\underline{\;微生物\;}}{\;}$2HCO3-+2NH3.
(4)K2FeO4能非常充分的去除救援产生的废水(以下简称救援废水)中的CN-离子.根据K2FeO4加入的量,分别发生下列反应:
Ⅰ.3CN-+2FeO42-+5H2O¾→2Fe(OH)3+3CNO-+4OH-
Ⅱ.6CN-+10FeO42-+22H2O¾→10Fe(OH)3+6CO32-+3N2+14OH-
Ⅲ.3CN-+8FeO42-+17H2O¾→8Fe(OH)3+3CO32-+3NO2-+10OH-
Ⅳ.3CN-+10FeO42-+22H2O¾→10Fe(OH)3+3CO32-+3NO3-+14OH-
现取含CN-离子的救援废水,加入一定量的K2FeO4,控制溶液pH=11.2,反应10min后,CN-离子的去除率超过99%.(假定K2FeO4只与CN-反应)
| 实验 | CN- 浓度 | 加入救援废水中的K2FeO4 | ||
| 救援废水 | 残余 | 浓度 | 利用率 | |
| ① | 10mg/L | 0.082mg/L | 75mg/L | 67.14% |
(5)室温下,0.1mol/L的氯化铵溶液和0.1mol/L的硫酸氢铵溶液,酸性更强的是NH4HSO4,
其原因是HSO4-有较大程度的电离,使溶液呈较强酸性.而NH4Cl只是NH4+水解呈弱酸性.已知:H2SO4:Ki2=1.2×10-2NH3•H2O:Ki=1.8×10-5.
1.下列物质的使用不涉及化学变化的是( )
| A. | 明矾用作净水剂 | B. | 铝镁合金材料制造飞机 | ||
| C. | 常温下,铁槽车运输浓硝酸 | D. | 用铝热反应焊接钢轨 |
8.不用外加试剂把下列溶液鉴别出来的先后顺序正确的是( )
①CuCl2
②NaNO3
③MgCl2
④NaOH.
①CuCl2
②NaNO3
③MgCl2
④NaOH.
| A. | ①②③④ | B. | ①③④② | C. | ④①②③ | D. | ①④③② |
2. 某同学在一张pH试纸上滴几滴新制的氯水,现象如图所示,下列有关该实验的说法中正确的是( )
某同学在一张pH试纸上滴几滴新制的氯水,现象如图所示,下列有关该实验的说法中正确的是( )
 某同学在一张pH试纸上滴几滴新制的氯水,现象如图所示,下列有关该实验的说法中正确的是( )
某同学在一张pH试纸上滴几滴新制的氯水,现象如图所示,下列有关该实验的说法中正确的是( )| A. | 该实验说明H+的扩散速度比HClO分子快 | |
| B. | 实验说明Cl2分子具有漂白性 | |
| C. | 将实验后的pH试纸在酒精灯上微热,试纸又恢复为原来颜色 | |
| D. | 若用久置的氯水进行上述实验,现象完全相同 |
3.化学与科学、技术、社会、环境密切相关.下列叙述中不正确的是( )
| A. | “血液透析”利用了胶体的性质 | |
| B. | 竹炭具有超强的吸附能力,能吸附新装修房屋内的有害气体 | |
| C. | 小苏打是制作馒头和面包等糕点的膨松剂,还是治疗胃酸过多的一种药剂 | |
| D. | 海水淡化可以解决淡水危机,向海水中加入明矾可以使海水淡化 |

 ,它在表中位置是③.(填“①”、“②”或“③”)该原子的最外层电子数为6
,它在表中位置是③.(填“①”、“②”或“③”)该原子的最外层电子数为6