题目内容
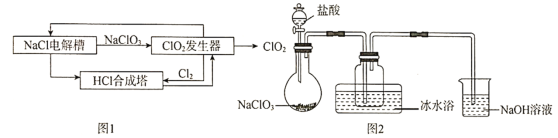
【题目】二氧化氯![]() 是一种高效、安全的消毒剂,常温下是一种黄绿色气体,11℃时液化成红棕色液体,易溶于水但不与水反应。工业上著名的开斯汀法制备二氧化氯的部分流程图如图1。某研究小组用图2装置模拟
是一种高效、安全的消毒剂,常温下是一种黄绿色气体,11℃时液化成红棕色液体,易溶于水但不与水反应。工业上著名的开斯汀法制备二氧化氯的部分流程图如图1。某研究小组用图2装置模拟![]() 发生器中的反应来制备
发生器中的反应来制备![]() (夹持装置已略去)
(夹持装置已略去)
(1)写出![]() 与盐酸反应的化学方程式。_____________
与盐酸反应的化学方程式。_____________
(2)冰水浴的作用是_____________。
(3)![]() 溶液中发生的主要反应的离子方程式为_______。
溶液中发生的主要反应的离子方程式为_______。
(4)将![]() 通入到
通入到![]() 溶液中,再向其中加入适量
溶液中,再向其中加入适量![]() ,振荡、静置,观察到_________,证明
,振荡、静置,观察到_________,证明![]() 具有氧化性。
具有氧化性。
(5)![]() 常用作自来水消毒剂,碘量法可以检测水中
常用作自来水消毒剂,碘量法可以检测水中![]() 的浓度,步骤如下:
的浓度,步骤如下:
①取![]() 水样,加入足量的碘化钾,再用氢氧化钠溶液调至中性,并加入淀粉溶液,溶液变蓝(已知
水样,加入足量的碘化钾,再用氢氧化钠溶液调至中性,并加入淀粉溶液,溶液变蓝(已知![]() 全部转化为
全部转化为![]() );
);
②用![]() 的
的![]() 溶液滴定,消耗
溶液滴定,消耗![]() 溶液
溶液![]() (已知:
(已知: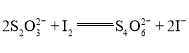 );
);
确定操作②达到滴定终点的现象是______;经计算,水样中![]() 的浓度是_________
的浓度是_________![]() 。
。
(6)一定温度和电压下,电解精制食盐水可制得![]() 和
和![]() 。
。
已知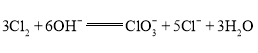 ,电解时应选用___交换膜(填“阳离子”或“阴离子”),阴极电极反应式为___。
,电解时应选用___交换膜(填“阳离子”或“阴离子”),阴极电极反应式为___。
【答案】2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O; 使![]() 冷凝为液体,收集
冷凝为液体,收集![]() 2OH-+Cl2=Cl-+ClO-+H2O 下层液体呈紫红色 溶液由蓝色变为无色,且半分钟内不变色 0.675 阴离子 2H2O+2e-=H2↑+2OH-
2OH-+Cl2=Cl-+ClO-+H2O 下层液体呈紫红色 溶液由蓝色变为无色,且半分钟内不变色 0.675 阴离子 2H2O+2e-=H2↑+2OH-
【解析】
(1) 在![]() 发生器中,
发生器中,![]() 和盐酸反应
和盐酸反应![]() 、氯气、氯化钠,根据得失电子守恒配平方程式;
、氯气、氯化钠,根据得失电子守恒配平方程式;
(2) 根据“![]() 常温下是一种黄绿色气体,11℃时液化成红棕色液体”分析;
常温下是一种黄绿色气体,11℃时液化成红棕色液体”分析;
(3)烧瓶中生成的氯气和氢氧化钠溶液反应生成氯化钠、次氯酸钠和水;
(4)将![]() 通入到
通入到![]() 溶液中,I-被氧化为I2;
溶液中,I-被氧化为I2;
(5) ①取![]() 水样,加入足量的碘化钾,再用氢氧化钠溶液调至中性,并加入淀粉溶液,溶液变蓝(已知
水样,加入足量的碘化钾,再用氢氧化钠溶液调至中性,并加入淀粉溶液,溶液变蓝(已知![]() 全部转化为
全部转化为![]() ),发生反应的离子方程式是2I-+2ClO2=I2+2ClO2-;用
),发生反应的离子方程式是2I-+2ClO2=I2+2ClO2-;用![]() 的
的![]() 溶液滴定,反应离子方程式是
溶液滴定,反应离子方程式是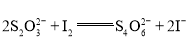 ,可得关系式ClO2 ~~
,可得关系式ClO2 ~~![]() ;
;
(6)电解时阴极发生还原反应生成氢气2H2O+2e-=H2↑+2OH-,阳极发生2Cl--2e-=Cl2,OH-向阳极移动,发生3Cl2+6OH-=ClO3-+5Cl-+3H2O,可制得NaClO3;
(1) 在![]() 发生器中,
发生器中,![]() 和盐酸反应
和盐酸反应![]() 、氯气、氯化钠,根据得失电子守恒,反应方程式为2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O;
、氯气、氯化钠,根据得失电子守恒,反应方程式为2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O;
(2) ![]() 常温下是一种黄绿色气体,11℃时液化成红棕色液体,所以冰水浴的作用是使
常温下是一种黄绿色气体,11℃时液化成红棕色液体,所以冰水浴的作用是使![]() 冷凝为液体,收集
冷凝为液体,收集![]() ;
;
(3)烧瓶中生成的氯气和氢氧化钠溶液反应生成氯化钠、次氯酸钠和水,反应的离子方程式是2OH-+Cl2=Cl-+ClO-+H2O;
(4)将![]() 通入到
通入到![]() 溶液中,I-被氧化为I2,再向其中加入适量
溶液中,I-被氧化为I2,再向其中加入适量![]() ,振荡、静置,观察到下层液体呈紫红色,证明
,振荡、静置,观察到下层液体呈紫红色,证明![]() 具有氧化性;
具有氧化性;
(5) 用![]() 的
的![]() 溶液滴定,达到滴定终点,碘完全消耗,现象是滴入最后一滴
溶液滴定,达到滴定终点,碘完全消耗,现象是滴入最后一滴![]() 溶液,溶液由蓝色变为无色,且半分钟内不变色;
溶液,溶液由蓝色变为无色,且半分钟内不变色;
设水样中![]() 的物质的量是xmol;
的物质的量是xmol;
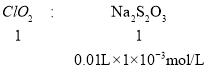
x=1×10-5mol,水样中![]() 的浓度是
的浓度是![]() 0.675
0.675![]() ;
;
(6)电解时阴极发生还原反应生成氢气,阴极反应式是2H2O+2e-=H2↑+2OH-,阳极发生2Cl--2e-=Cl2,OH-向阳极移动,发生3Cl2+6OH-=ClO3-+5Cl-+3H2O,可制得NaClO3,所以电解时应选用阴离子交换膜。

【题目】异丁烯![]() 是一种重要的化工原料,可由异丁烷
是一种重要的化工原料,可由异丁烷![]() 直接催化脱氢制备:
直接催化脱氢制备:
(1)已知:![]()
![]()
写出由异丁烷![]() 催化脱氢制备异丁烯
催化脱氢制备异丁烯![]() 的热化学方程式。_________。
的热化学方程式。_________。
(2)一定条件下,以异丁烷为原料催化脱氢生产异丁烯。温度、压强的改变对异丁烷平衡转化率的影响如图所示。

①判断![]() 、
、![]() 的大小关系:
的大小关系:![]() _____________
_____________![]() (填“>”或“<”);能使单位时间内异丁烯的产量提高,又能使异丁烷平衡产率提高,应采取的措施是____________(填标号)。
(填“>”或“<”);能使单位时间内异丁烯的产量提高,又能使异丁烷平衡产率提高,应采取的措施是____________(填标号)。
a.升高温度 b.降低温度 c.增大压强 d.降低压强 e.使用催化剂
②平衡常数的表达式中的平衡浓度可以用平衡时各气体的分压代替(气体a的分压=气体a的物质的量分数×总压强,即![]() (总)。求图中的A点状态下的异丁烷脱氢反应的平衡常数
(总)。求图中的A点状态下的异丁烷脱氢反应的平衡常数![]() _____________(保留两位有效数字)。
_____________(保留两位有效数字)。
(3)温度对催化剂的活性和目标产物的选择性都有一定的影响。下表是以![]() 为催化剂,在反应时间相同时,测得的不同温度下的数据。
为催化剂,在反应时间相同时,测得的不同温度下的数据。
温度/℃ | 550 | 570 | 590 | 610 | 630 |
异丁烷转化率/% | 13.8 | 24.5 | 25.6 | 30.0 | 33.3 |
异丁烯选择性/% | 93.9 | 88.3 | 95.0 | 80.4 | 71.2 |
异丁烯的产率/% | 12.9 | 21.6 | w | 24.1 | 23.7 |
已知①选择性![]() ;②异丁烷高温下裂解生成短碳链烃类化合物
;②异丁烷高温下裂解生成短碳链烃类化合物
①590℃时异丁烯的产率![]() _____________×100%。
_____________×100%。
②在590℃之前异丁烯的产率随温度升高而增大的原因可能是____________、_____________。
③590℃之后,异丁烯产率降低的主要原因可能是_____________。