题目内容
【题目】COCl2(g)![]() CO(g)+Cl2(g) ΔH>0,当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,能提高COCl2转化率的是
CO(g)+Cl2(g) ΔH>0,当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,能提高COCl2转化率的是
A.①②④B.②③⑤C.①④⑥D.③⑤⑥
【答案】C
【解析】
根据化学方程式可知,反应是体积增大的、吸热的可逆反应,所以升高温度或降低压强,反应都是向正反应方向进行的,COCl2转化率增大,①④正确;
②恒容通入惰性气体,浓度不变,平衡不移动转化率不变,错误;
③增加CO的浓度,平衡向逆反应方向移动,转化率降低,错误;
⑤催化剂不能改变平衡状态,转化率不变,错误;
⑥恒压通入惰性气体,则容积增大,平衡向正反应方向移动,COCl2转化率增大,正确;
综上所述,①④⑥正确;
答案选C。

【题目】市场销售的某种食用精制盐包装袋上有如下说明:
产品标准 | GB5461 |
产品等级 | 一级 |
配 料 | 食盐、碘酸钾、抗结剂 |
碘含量 | 20~50mg/kg |
(1)碘酸钾与碘化钾在酸性条件下发生如下反应,配平化学方程式![]() 将化学计量数填于空白处
将化学计量数填于空白处![]()
______ ![]() ______
______ ![]() ______
______ ![]() ______
______ ![]() ______
______ ![]() ______
______ ![]()
(2)已知:![]() 某学生测定食用精制盐的碘含量,其步骤为:
某学生测定食用精制盐的碘含量,其步骤为:
![]() 准确称取12.7g食盐,加适量蒸馏水使其完全溶解;
准确称取12.7g食盐,加适量蒸馏水使其完全溶解;
![]() 用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全;
用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全;
![]() 以淀粉为指示剂,逐滴加入物质的量浓度为6.0×10-4molL-1的Na2S2O2溶液20.0mL,恰好反应完全.
以淀粉为指示剂,逐滴加入物质的量浓度为6.0×10-4molL-1的Na2S2O2溶液20.0mL,恰好反应完全.
![]() 判断c中反应恰好完全依据的现象是 ______ .
判断c中反应恰好完全依据的现象是 ______ .
![]() 根据以上实验和包装袋说明,所测精制盐的碘含量是 ______mg/kg.
根据以上实验和包装袋说明,所测精制盐的碘含量是 ______mg/kg.
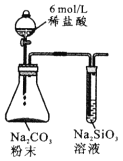
【题目】由下列实验现象一定能得出相应结论的是
选项 | A | B | C | D |
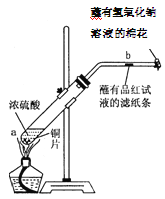
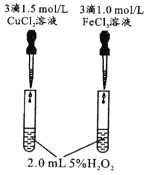
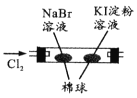
装置图 |
|
|
|
|
现象 | 右边试管产生气泡较快 | 左边棉球变棕黄色,右边棉球变蓝色 | 试管中先出现淡黄色固体,后出现黄色固体 | 试管中液体变浑浊 |
结论 | 催化活性:Fe3+>Cu2+ | 氧化性:Br2>I2 | Ksp:AgCl>AgBr>AgI | 非金属性:C>Si |
A. AB. BC. CD. D