题目内容
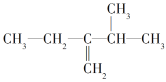
【题目】链烃A的核磁共振氢谱显示只含有一种氢原子,A的质谱图中显示其最大质荷比为84,A的红外光谱表明分子中含有碳碳双键。
(1)A的结构简式为____。
(2)在图中,D1、D2互为同分异构体,E1、E2互为同分异构体。
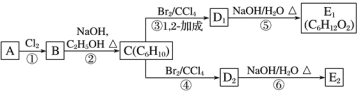
C的化学名称是___;反应⑤的化学方程式为____;E2的结构简式是____;②、⑥的反应类型依次____、___。
【答案】(CH3)2C=C(CH3)2 2,3-二甲基-1,3-丁二烯 CH2BrCBr(CH3)C(CH3)=CH2+2NaOH![]() HOCH2C(OH)(CH3)C(CH3)=CH2+2NaBr HOCH2C(CH3)=C(CH3)CH2OH 消去反应 取代反应
HOCH2C(OH)(CH3)C(CH3)=CH2+2NaBr HOCH2C(CH3)=C(CH3)CH2OH 消去反应 取代反应
【解析】
链烃A的质谱图表明其相对分子质量为84,令组成为CxHy,则x最大值为![]() =7,红外光谱表明分子中含有碳碳双键,所以A为烯烃,所以x=6,y=12,因此A的化学式为C6H12,核磁共振氢谱表明分子中只有一种类型的氢,故A的结构简式为(CH3)2C=C(CH3)2,A与氯气反应生成B,B为(CH3)2CClCCl(CH3)2,B在氢氧化钠、乙醇作用下加热,发生消去反应生成C,C为CH2=C(CH3)C(CH3)=CH2,C与溴发生1,2-加成生成D1,故D1为CH2BrCBr(CH3)C(CH3)=CH2,D1在氢氧化钠水溶液中发生水解反应生成E1,E1为HOCH2C(OH)(CH3)C(CH3)=CH2,D1、D2互为同分异构体,故反应④发生1,4-加成,D2为CH2BrC(CH3)=C(CH3)CH2Br,D2在氢氧化钠水溶液中发生水解反应生成E2,E2为HOCH2C(CH3)=C(CH3)CH2OH,
=7,红外光谱表明分子中含有碳碳双键,所以A为烯烃,所以x=6,y=12,因此A的化学式为C6H12,核磁共振氢谱表明分子中只有一种类型的氢,故A的结构简式为(CH3)2C=C(CH3)2,A与氯气反应生成B,B为(CH3)2CClCCl(CH3)2,B在氢氧化钠、乙醇作用下加热,发生消去反应生成C,C为CH2=C(CH3)C(CH3)=CH2,C与溴发生1,2-加成生成D1,故D1为CH2BrCBr(CH3)C(CH3)=CH2,D1在氢氧化钠水溶液中发生水解反应生成E1,E1为HOCH2C(OH)(CH3)C(CH3)=CH2,D1、D2互为同分异构体,故反应④发生1,4-加成,D2为CH2BrC(CH3)=C(CH3)CH2Br,D2在氢氧化钠水溶液中发生水解反应生成E2,E2为HOCH2C(CH3)=C(CH3)CH2OH,
(1)由上述分析可知,A的结构简式为:(CH3)2C=C(CH3)2;
答案为(CH3)2C=C(CH3)2。
(2)C为CH2=C(CH3)C(CH3)=CH2,则化学名称是2,3-二甲基-1,3-丁二烯;反应⑤的化学方程式为CH2BrCBr(CH3)C(CH3)=CH2+2NaOH ![]() HOCH2C(OH)(CH3)C(CH3)=CH2+2NaBr;E2的结构简式是HOCH2C(CH3)=C(CH3)CH2OH,②的反应类型消去反应,⑥的反应类型取代反应;
HOCH2C(OH)(CH3)C(CH3)=CH2+2NaBr;E2的结构简式是HOCH2C(CH3)=C(CH3)CH2OH,②的反应类型消去反应,⑥的反应类型取代反应;
答案为2,3-二甲基-1,3-丁二烯,CH2BrCBr(CH3)C(CH3)=CH2+2NaOH ![]() HOCH2C(OH)(CH3)C(CH3)=CH2+2NaBr,HOCH2C(CH3)=C(CH3)CH2OH,消去反应,取代反应。
HOCH2C(OH)(CH3)C(CH3)=CH2+2NaBr,HOCH2C(CH3)=C(CH3)CH2OH,消去反应,取代反应。

【题目】下表是几种弱酸常温下的电离平衡常数:
CH3COOH | H2CO3 | H2S | H3PO4 |
1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | K1=9.1×10-8 K2=1.1×10-12 | K1=7.5×10-3 K2=6.2×10-8 K3=2.2×10-13 |
则下列说法中不正确的是( )
A. 碳酸的酸性强于氢硫酸
B. 多元弱酸的酸性主要由第一步电离决定
C. 常温下,加水稀释醋酸,![]() 增大
增大
D. 向弱酸溶液中加少量NaOH溶液,电离常数不变
【题目】1,2-二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,不溶于水,易溶于醇等有机溶剂。实验室制备1,2-二溴乙烷的反应原理如下:
CH3CH2OH![]() CH2=CH2+H2O
CH2=CH2+H2O
CH2=CH2+Br2→BrCH2CH2Br
已知:①乙醇在浓硫酸存在下在140℃脱水生成乙醚
2CH3CH2OH![]() CH3CH2OCH2CH3+H2O
CH3CH2OCH2CH3+H2O
②实验中常因温度过高而使乙醇和浓硫酸反应生成少量SO2和CO2,用12.0g溴和足量的乙醇制备1,2-二溴乙烷,实验装置如图所示:
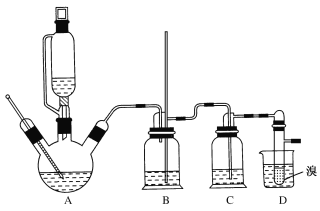
有关数据列表如下:
类别 | 乙醇 | 1,2-二溴乙烷 | 乙醚 |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/g·cm-3 | 0.79 | 2.2 | 0.71 |
沸点/℃ | 78.5 | 132 | 34.6 |
熔点/℃ | -130 | 9 | -116 |
回答下列问题:
(1)在此制备实验中,A中按最佳体积比3﹕1加入乙醇与浓硫酸后,A中还要加入几粒碎瓷片,其作用是___。要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是___。
(2)装置B的作用是作安全瓶,瓶中盛水,除了可以防止倒吸以外,还可判断装置是否堵塞,若堵塞,B中现象是____。
(3)在装置C中应加入NaOH溶液,其目的是____。
(4)装置D中小试管内盛有液溴,判断该制备反应已经结束的最简单方法是___。
(5)将1,2—二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在___层(填“上”或“下”)。若产物中有少量未反应的Br2,最好用___洗涤除去;若产物中有少量副产物乙醚,可用____(填操作方法名称)的方法除去。
(6)反应过程中应用冷水冷却装置D,其主要目的是乙烯与溴反应时放热,冷却可避免溴的大量挥发;但又不能过度冷却(如用冰水),其原因是___。
(7)若实验结束后得到9.4g产品,1,2—二溴乙烷的产率为___。