��Ŀ����
����Ŀ����Ũ����ȡ������Ϊ50mL��A��B����NaOH��Һ�У���ͨ��һ������CO2����ϡ�͵�100mL����ϡ�ͺ����Һ����μ���0.1mol/L�����ᣬ����CO2���������״��������������������ϵ����ͼ��ʾ��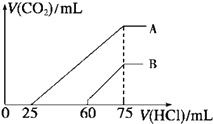
��A���߱�����ԭ��Һͨ��CO2���������������ᷴӦ����CO2����������mL����״������
��B���߱�����ԭ��Һͨ��CO2��������Һ�����ʵĻ�ѧʽΪ���ʵ���֮��Ϊ��
��ԭNaOH��Һ�����ʵ���Ũ��Ϊ ��
���𰸡�112��Na2CO3��NaHCO3��1��1��0.15mol/L
���������⣺��ͼ��֪����ӦB��Һ��˵���μ�����60mLʱû���������ɣ����ܷ���OH��+H+=H2O��CO32��+H+=HCO3�� �� ����ԭ��Һ��ֻ��̼���ƣ�����̼��������Ҫ����������̼�����������Ȼ�����Ҫ����������ȣ�ʵ������Ҫ��������60mLԶԶ����̼�����������Ȼ�����Ҫ����������75��60��mL=15mL��˵��ԭ��Һ�е�������NaOH��Na2CO3������A��Һ��˵���μ�����25mLʱû���������ɣ����ܷ���OH��+H+=H2O��CO32��+H+=HCO3�� �� ����ԭ��Һ��ֻ��̼���ƣ�����̼��������Ҫ����������̼�����������Ȼ�����Ҫ����������ȣ�ʵ������Ҫ��������25mLС��̼�����������Ȼ�����Ҫ����������75��25��mL=50mL��˵��ԭ��Һ�е�������Na2CO3��NaHCO3 �� �ٶ���A��Һ��˵���μ�����25mLʱ���������ɣ���μ���0.1molL��1 �����ᣬ������CO2����ʱ��������ӦHCO3��+H+=H2O+CO2������HCO3��+H+=H2O+CO2��
11
n��CO2��=0.05L��0.1mol/L=0.005mol����������Ϊ0.005mol��22.4L/mol=0.112L=112mL��
���Դ��ǣ�112��
��������������֪��B��������Na2CO3��NaHCO3 �� ����������Ĺ�ϵ��֪�����ߵ����ʵ�����ͬ�������ʵ�����Ϊ1��1�����Դ��ǣ�Na2CO3��NaHCO3��1��1���ۼ�����������������Һ�о�ֻ����NaCl��n��HCl��=n��NaOH��=0.075L��0.1mol/L=0.0075mol��c��NaOH��= ![]() =
= ![]() =0.15mol/L��
=0.15mol/L��
���Դ��ǣ�0.15mol/L��