题目内容
【题目】铝氢化钠(NaAlH4)是有机合成的重要还原剂,其合成路线如图所示。
![]()
(1)已知AlCl3的熔点为190℃,沸点为178℃,在湖湿的空气中易水解。某实验小组利用下图中装置制备无水AlCl3。
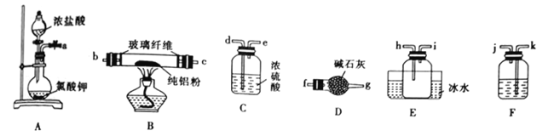
①写出圆底烧瓶中发生反应的离子方程式:_________________。
②按气流方向连接各仪器接口,顺序为a→__________b→c→_______。 (填接口字母)
③装置F中应盛装的试剂是__________,装置D的作用是______________。
(2)AlCl3与NaH反应时,需先将AlCl3溶于有机溶剂,再将得到的溶液滴加到NaH粉末中,此反应中NaH的转化率较低,其原因可能是______________。
(3)通过测定铝氢化钠与水反应生成氢气的体积来测定铝氢化钠样品的纯度。
①铝氢化的与水反应的化学方程式为______________。
②设计如下四种装置测定铝氢化钠样品的纯度(杂质只有氢化钠)。从简约性、准确性考虑,最恰当的装置是___(填编号)。
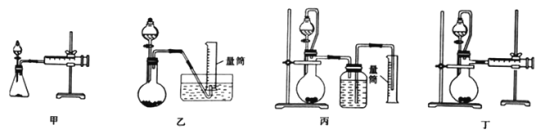
③某同学选用上述最恰当的裴置,称取mg铝氢化钠样品,测得生成气体的体积为VL(已折算为标准状况),重复实验操作三次,测得有关数据如下表所示,则样品中铝氢化钠的纯度为____。
实验次数 | 样品质量m(g) | 气体休积V(L) |
I | 1.20 | 1.907 |
II | 1.20 | 1.904 |
III | 1.20 | 1,901 |
【答案】 5Cl-+ClO3-+6H+=3Cl2↑+3H2O k→j→d→e h→i→f→g 饱和NaCl溶液 吸收未反应的Cl2,并防止空气中的水蒸气进入装置E中 NaH是离子化合物,难溶于有机溶剂,使反应物难以接触(或其他合理答案) NaAlH4+2H2O=NaAlO2+4H2↑ 丁 90.0%
【解析】(1)①圆底烧瓶中浓盐酸与氯酸钾反应生成氯化钾、氯气和水,发生反应的离子方程式为: 5Cl-+ClO3-+6H+=3Cl2↑+3H2O;②A装置制得氯气,通过F除去氯化氢,再通过C干燥,纯净干燥的氯气与铝粉在B中反应,产生的氯化铝在E中冷却而得,最后装置D防止空气中的水蒸气进入E。按气流方向连接各仪器接口,顺序为a→k→j→d→e →b→c→h→i→f→g;③装置F中应盛装的试剂是为了除去反应挥发出的氯化氢,为饱和NaCl溶液;装置D的作用是吸收未反应的Cl2,并防止空气中的水蒸气进入装置E中;(2)AlCl3与NaH反应时,需先将AlCl3溶于有机溶剂,再将得到的溶液滴加到NaH粉末中,此反应中NaH的转化率较低,其原因可能是NaH是离子化合物,难溶于有机溶剂,使反应物难以接触;(3) ①铝氢化的与水反应生成偏铝酸钠和氢气,反应的化学方程式为NaAlH4+2H2O=NaAlO2+4H2↑;②测定铝氢化钠的纯度,就是利用其与水反应生成氢气,测定氢气的体积,所以给的装置中丁的装置可以较准确的测定氢气的体积,所以选择丁。甲中锥形瓶中的压强变大,可能液体不能顺利流下,铝氢化钠或许不能完全反应,丙装置中导管中可能有水,使测定的气体的体积不准确,乙的操作中氢气的体积不好读数;答案选丁;③产生气体的体积平均值为![]() ,根据反应NaAlH4+2H2O=NaAlO2+4H2↑可知,样品中铝氢化钠的纯度为
,根据反应NaAlH4+2H2O=NaAlO2+4H2↑可知,样品中铝氢化钠的纯度为![]() 。
。

 阅读快车系列答案
阅读快车系列答案【题目】亚硝酰氯(ClNO)是有机合成中的重要试剂,在工业上有重要的用途。
(1)已知:4HCl(g)+O2(g)=2Cl2(g)+2H2O(g) △H1;
2ClNO(g)+H2O(g)=NO(g)+2HCl(g ) △H2。
则反应:4ClNO(g)+O2(g)=2Cl2(g)+2N2O3(g)的△H=_______(用含△H1、△H2 的代数式表示 )。
(2)将NO与Cl2按物质的量之比2:1充入一绝热密闭容器中,发生反应:
2NO(g)+Cl2(g) ![]() 2ClNO(g) △H<0,实验测得NO的转化率α(NO)随时间的变化如图所示。
2ClNO(g) △H<0,实验测得NO的转化率α(NO)随时间的变化如图所示。
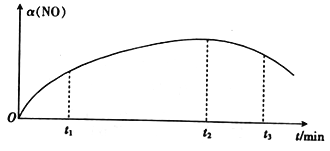
NO(g)的转化率α(NO)在t2~t3时间段内降低的原因是___________。
(3)在其他条件相同时,向五个恒温恒容的密闭容器中分别充入1mol Cl2 与2 mol NO,发生反应:2NO(g)+Cl2(g)![]() 2ClNO(g) △H<0,部分反应条件及平衡时Cl2 的转化率如下表所示。
2ClNO(g) △H<0,部分反应条件及平衡时Cl2 的转化率如下表所示。
容器编号 | 温度/℃ | 容器体积/L | 平衡时Cl2 的转化率 |
I | T1 | 2 | 75% |
II | T2=T1 | 3 | ω2 |
Ⅲ | T3>T1 | V3 | 75 % |
Ⅳ | T4 | V4 | ω4 |
V | T5 | V5 | ω5 |
①6 min时容器I中反应达到平衡,则0~6 min内,v(NO)=______mol·L-l·min-1。
②V3______(填“ > ”“<”或“ = ”) 2。
③容器I中反应的平衡常数的值K2=______,容器Ⅲ中反应的平衡常数的值K3=_____(填“>”“<”或“=”)K2。
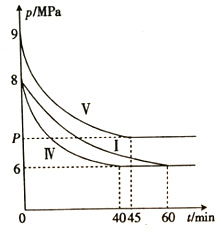
④容器Ⅳ、容器V分别与容器I相比只有一个实验条件不同,反应体系总压强随时间的变化如图所示。与容器I相比,容器Ⅳ改变的实验条件是_______;容器V与容器I 的体积不同,则容器V中反应达到平衡时气体总压强(P)的范围是________。