题目内容
19.下列说法或表示方法中正确的是( )| A. | 等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 | |
| B. | 由C(金刚石)→C(石墨);△H=-1.9KJ/mol 可知,金刚石比石墨稳定 | |
| C. | 在101Kpa时,2gH2完全燃烧生成液态水,放出285.8KJ热量,氢气燃烧的热化学方程式为:2H2(g)+O2(g)=2H2O(l);△H=+285.8KJ/mol | |
| D. | 稀溶液中:H+(aq)+OH-(aq)=H2O(l);△H=-53.7KJ/mol,若将含0.5 molH2SO4的浓溶液与含1 molNaOH的溶液混合,放出的热量大于53.7KJ/mol |
分析 A、硫蒸气变化为硫固体为放热过程;
B、物质的能量越低越稳定;
C、燃烧热为放热,焓变为负值;
D、浓硫酸溶于水放热.
解答 解:A、硫蒸气变化为硫固体为放热过程,则等量的硫蒸气和硫固体在氧气中分别完全燃烧,放出热量硫蒸气多,即前者放出热量多,故A正确;
B、石墨能量比金刚石低,石墨稳定,故B错误;
C、燃烧热为放热,焓变为负值,故C错误;
D、浓硫酸溶于水放热,所以0.5 mol H2SO4的浓硫酸与含1 mol NaOH的溶液混合,整个过程放出的热量大于57.3 kJ,故D正确;
故选AD.
点评 本题考查了化学反应中的能量变化,燃烧热、中和热的概念,属于基础知识的考查,题目难度不大.

练习册系列答案
相关题目
10.PASS是新一代高效净水剂,它由X、Y、Z、W、R五种短周期元素组成,五种元素原子序数依次增大.X原子是所有原子中半径最小的,Y、R同主族,Z、W、R同周期,Y原子的最外层电子数是次外层的3倍,Z是常见的金属,电子层数等于主族序数,W单质是人类将太阳能转变为电能的常用材料.下列说法正确的是( )
| A. | 原子半径按X、Y、Z、R、W的顺序依次增大 | |
| B. | 熔沸点:X2R>X2Y | |
| C. | Z与Y形成的化合物可作为耐高温材料 | |
| D. | WY2能与碱反应,但不能与任何酸反应 |
14.下列四个能级中,能量最高,电子最后填充的是( )
| A. | 3s | B. | 3p | C. | 3d | D. | 4s |
4.下列关于溶液中离子的说法正确的是( )
| A. | 0.1 mol•L-1的Na2CO3溶液中离子浓度关系:c (Na+)=2c (CO32-)+c (HCO3-)+c (H2CO3) | |
| B. | 0.1 mol•L-1的NH4Cl和0.1 mol•L-1的NH3•H2O等体积混合后溶液中的离子浓度关系:c (Cl-)>c (NH4+)>c (H+)>c (OH-) | |
| C. | 常温下,醋酸钠溶液中滴加少量醋酸使溶液的pH=7,则混合溶液中,离子浓度关系:c (Na+)>c (CH3COO-) | |
| D. | 0.1 mol•L-1的NaHS溶液中离子浓度关系:c (OH-)=c (H+)-c (S2-)+c (H2S) |
8.在盛有NaOH溶液的试剂瓶口常看到白色固体生成,该固体是( )
| A. | Na2O | B. | NaOH | C. | NaHCO3 | D. | Na2CO3 |
9.某个原子的质量为a g,设NA表示阿伏加德罗常数,则该原子的相对原子质量( )
| A. | aNA | B. | $\frac{a}{{N}_{A}}$ | C. | $\frac{{N}_{A}}{a}$ | D. | $\frac{a}{{N}_{A}}$×6.02×1023 |
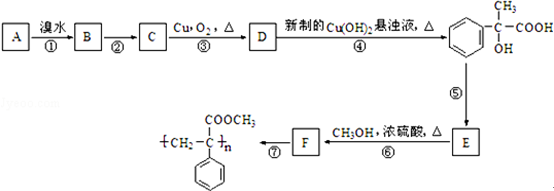
 ;F
;F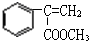
 .
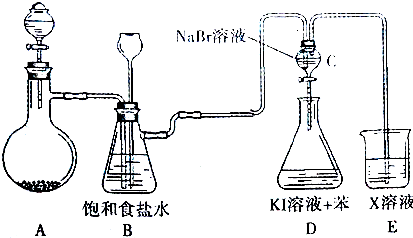
.
 .
.