题目内容
8.在盛有NaOH溶液的试剂瓶口常看到白色固体生成,该固体是( )| A. | Na2O | B. | NaOH | C. | NaHCO3 | D. | Na2CO3 |
分析 NaOH具有碱性,可与空气中CO2反应生成Na2CO3,以此解答.
解答 解:NaOH具有碱性,空气中能与NaOH反应的主要物质为CO2,发生:2NaOH+CO2=Na2CO3+H2O,以Na2CO3•10H2O的形成存在,最后风化生成Na2CO3,
故选D.
点评 本题考查钠的化合物的性质,为高频考点,题目难度不大,本题注意把握空气的成分以及钠的常见化合物的性质.

练习册系列答案
相关题目
18.下列说法正确的是( )
| A. | 废旧电池不能混到生活垃圾中,可以用焚烧的方法处理 | |
| B. | 防腐剂能延长食品的保存期,所以应大量使用防腐剂 | |
| C. | 84消毒液属于含氯消毒剂,和食品一样有保质期 | |
| D. | 臭氧具有优异的杀菌消毒功能,在居室内保持低浓度的臭氧是有益的 |
19.下列说法或表示方法中正确的是( )
| A. | 等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 | |
| B. | 由C(金刚石)→C(石墨);△H=-1.9KJ/mol 可知,金刚石比石墨稳定 | |
| C. | 在101Kpa时,2gH2完全燃烧生成液态水,放出285.8KJ热量,氢气燃烧的热化学方程式为:2H2(g)+O2(g)=2H2O(l);△H=+285.8KJ/mol | |
| D. | 稀溶液中:H+(aq)+OH-(aq)=H2O(l);△H=-53.7KJ/mol,若将含0.5 molH2SO4的浓溶液与含1 molNaOH的溶液混合,放出的热量大于53.7KJ/mol |
3.设NA代表阿伏加德罗常数,下列对于0.3mol/L的H2SO4溶液的说法不正确的是( )
| A. | 2L溶液中含有0.6NA个SO42-离子 | |
| B. | 2L溶液中H+离子的浓度为1.2mol/L | |
| C. | 1L溶液中含有H+离子0.6mol | |
| D. | 1L溶液中含溶质阴阳离子的总数为0.9NA个 |
13.下列氧原子的电子排布图中,正确的是( )
| A. | 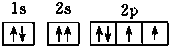 | B. | 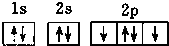 | ||
| C. | 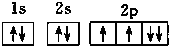 | D. | 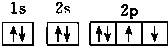 |
20.在一定条件下,对反应4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H<0,下列叙述正确的是( )
| A. | 3v(NH3)=2v(H2O) | |
| B. | 在此条件下,该反应不一定能自发进行 | |
| C. | 达到化学平衡时,若增加容器体积,则正反应速率减小,逆反应速率增大 | |
| D. | 若降低温度,达到新的化学平衡时,NO的体积分数将增大 |
17.用NA表示阿伏伽德罗常数的值,下列判断正确的是( )
| A. | 8g O2含有4NA个电子 | |
| B. | 1L 1mol•L-1的H2SO4溶液所含氧原子数为4NA | |
| C. | 标准状况下,22.4L O2和CO2的混合气体所含原子数为2.5NA | |
| D. | 标准状况下,22.4L CCl4含有NA个分子 |
18.反应 A+B→C 的反应速率方程式为:v=k•c(A)•c(B),v为反应速率,k为速率常数.当c(A)=c(B)=1mol/L时,反应速率在数值上等于速率常数.下列说法正确的是( )
| A. | c(A)增大时,v也增大 | B. | c(B)增大时,k也增大 | ||
| C. | 升高温度时,k值不变 | D. | 升高温度时,v值增大 |