题目内容
【题目】对燃煤烟气和汽车尾气进行脱硝、脱碳和脱硫等处理,可实现绿色环保、节能减排等目的。汽车尾气脱硝脱碳的主要原理为:2NO(g)+2CO(g)![]() N2(g)+2CO2(g)△H=-Q(Q>0)。一定条件下,在一密闭容器中,用传感器测得该反应在不同时间的NO和CO浓度如下表:
N2(g)+2CO2(g)△H=-Q(Q>0)。一定条件下,在一密闭容器中,用传感器测得该反应在不同时间的NO和CO浓度如下表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
c(NO)/mol·L-1 | 1.00×10-3 | 4.50×10-4 | 2.50×10-4 | 1.50×10-4 | 1.00×10-4 | 1.00×10-4 |
c(CO)/mol·L-1 | 3.60×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |
(1)写出该反应的平衡常数表达式____________________。
(2)前2s内的平均反应速率υ(N2)=__________;达到平衡时,CO的转化率为___________。
(3)采用低温臭氧氧化脱硫脱硝技术,同时吸收SO2和NOx,获得(NH4)2SO4的稀溶液,往(NH4)2SO4溶液中再加入少量 (NH4)2SO4固体, 的值将_______(填 “变大”、“不变”或“变小”)。
的值将_______(填 “变大”、“不变”或“变小”)。
【答案】K= 1.875×10-4mol/(L·s) 25.0% 变大
1.875×10-4mol/(L·s) 25.0% 变大
【解析】
(1)根据化学平衡常数等于平衡时各种生成物浓度幂之积与各种反应物浓度幂之积的比书写平衡常数表达式;
(2)先根据前2s内NO的浓度变化计算N2的浓度变化,然后根据v(N2)=![]() 计算反应速率;根据达到平衡时CO的转变浓度除以反应开始时CO的总浓度可得CO的转化率;
计算反应速率;根据达到平衡时CO的转变浓度除以反应开始时CO的总浓度可得CO的转化率;
(3)根据盐的浓度越大,盐水解程度降低分析判断。
(1)由于化学平衡常数等于平衡时各种生成物浓度幂之积与各种反应物浓度幂之积的比,所以该反应的化学平衡常数表达式K= ;
;
(2)由表格数据可知反应前2s内NO的转化浓度7.50×10-4mol/L,由反应方程式可知:每反应消耗2mol/LNO,反应产生1mol/LN2,则N2的转化浓度为7.50×10-4mol/L÷2=3.75×10-4mol/L,则用N2表示的前2s内的反应速率为v(N2)= 3.75×10-4mol/L÷2s=1.875×10-4mol/(L·s);
反应开始时CO的浓度为3.60×10-3mol/L,达到平衡时CO的浓度为2.70×10-3mol/L,则CO反应消耗浓度为3.60×10-3mol/L-2.70×10-3mol/L=9.00×10-4mol/L,所以CO的转化率为[9.00×10-4mol/L÷(3.60×10-3mol/L)]×100%=25.0%;
(3)(NH4)2SO4是强酸弱碱盐,在溶液中NH4+发生水解反应而消耗,使溶液显酸性,往(NH4)2SO4溶液中再加入少量 (NH4)2SO4固体,即增大了的(NH4)2SO4浓度,盐水解程度降低,所以溶液中 的值将变大。
的值将变大。

 百年学典课时学练测系列答案
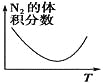
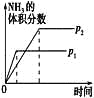
百年学典课时学练测系列答案【题目】对于可逆反应N2(g)+3H2(g)![]() 2NH3(g) ΔH<0。下列研究目的和图示相符的是
2NH3(g) ΔH<0。下列研究目的和图示相符的是
A | B | C | D | |
研究目的 | 温度(T)对反应的影响(T2>T1) | 压强(p)对平衡常数的影响 | 温度(T)对反应的影响 | 压强(p)对反应的影响(p2>p1) |
图示 |
|
|
|
|
A.AB.B .C.CD.D