题目内容
20.下列说法正确的是( )①常温下,强酸溶液的pH=a,将溶液的体积稀释到原来10n,则pH=a+n
②已知BaSO4的Ksp=c(Ba2+)•c(SO42-),所以在BaSO4溶液中有c(Ba2+)=c(SO42-)=$\sqrt{{K}_{sp}}$
③将0.1mol•L-1的NaHS和0.1mol•L-1 Na2S溶液等体积混合,所得溶液中有c(S2-)+2c(OH-)=2c(H+)+c(HS-)+3c(H2S)
④在0.1mol•L-1氨水中滴加0.1mol•L-1盐酸,刚好完全中和时pH=a,由水电离产生的c(OH+ )=10-amol•L-1.
| A. | ①④ | B. | ②③ | C. | ③④ | D. | ①② |
分析 ①若a+n<7时,常温下,强酸溶液的pH=a,将溶液的体积稀释到原来10n倍,则pH=a+n;但是若a+n≥7时,溶液稀释后其pH不可能大于7,只能无限接近7;
②对于饱和溶液,在BaSO4溶液中有c(Ba2+)=c(SO42-)=$\sqrt{{K}_{sp}}$,若溶液不饱和,该关系不成立;
③根据0.1mol•L-1的NaHS和0.1mol•L-1 Na2S混合溶液中物料守恒和电荷守恒进行判断;
④刚好完全中和时,氢离子与氢氧根离子浓度相等,pH=a的溶液中c(H+)=c(OH-)=10-amol•L-1;
解答 解:①常温下,强酸溶液的pH=a,将溶液的体积稀释到原来10n倍,若a+n<7时,则pH=a+n;但是若a+n≥7时,溶液稀释后其pH不可能大于7,溶液的pH只能无限接近7,故①错误;
②已知BaSO4的Ksp=c(Ba2+)•c(SO42-),对于饱和溶液BaSO4溶液中,则有c(Ba2+)=c(SO42-)=$\sqrt{{K}_{sp}}$,但是若溶液不是饱和溶液,该关系不会成立,故②错误;
③将0.1mol•L-1的NaHS和0.1mol•L-1 Na2S溶液等体积混合,根据物料守恒可得:2c(Na+)=3[c(HS-)+c(H2S)+c(S2-)],根据电荷守恒可知:c(H+)+c(Na+)=2c(S2-)+c(OH-)+c(HS-),由电荷守恒和物料守恒联立可得:c(S2-)+2c(OH-)=2c(H+)+c(HS-)+3c(H2S),故③正确;
④在0.1mol•L-1氨水中滴加0.1mol•L-1盐酸,刚好完全中和时pH=a,则溶液中c(OH-)=c(H+)=10-amol•L-1,故④正确;
故选C.
点评 本题考查了溶液pH的计算、溶液中离子浓度大小比较、难溶电解质的沉淀平衡等知识,题目难度中等,注意掌握酸碱混合后溶液的定性判断及溶液中pH的计算方法,明确酸溶液稀释后不可能变成碱溶液,常温下溶液的pH只能无限接近7;学会利用电荷守恒、物料守恒、盐的水解原理比较溶液中离子浓度大小.

| A. | Al(OH)3能溶于NaOH溶液,而Mg(OH)2不能 | |
| B. | 铝的原子半径比镁小 | |
| C. | 镁与浓硫酸反应,铝与冷的浓硫酸不反应 | |
| D. | 铝的金属光泽不如镁显著 |
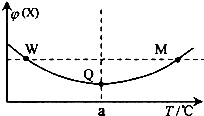 在某2L恒容密闭容器中充入2mol X(g)和1mol Y(g)发生反应:2X(g)+Y(g)═3Z(g)△H,反应过程中持续升高温度,测得混合体系中X的体积分数与温度的关系如右图所示.下列推断正确的是( )
在某2L恒容密闭容器中充入2mol X(g)和1mol Y(g)发生反应:2X(g)+Y(g)═3Z(g)△H,反应过程中持续升高温度,测得混合体系中X的体积分数与温度的关系如右图所示.下列推断正确的是( )| A. | M点时,Y的转化率最大 | |
| B. | 升高温度,平衡常数减小 | |
| C. | 平衡后充入Z达到新平衡时Z的体积分数增大 | |
| D. | W,M两点Y的正反应速率相等 |
| A. | 正反应的活化能比逆反应的活化能大234kJ•mol-1 | |
| B. | NO3是该反应的催化剂 | |
| C. | 化学反应速率v(NO2)=2v(CO) | |
| D. | 过程1和过程2均为放热反应 |

| A. | 分子中所有原子在同一平面上 | |
| B. | 分子中含有2种官能团 | |
| C. | 可发生加成和取代反应 | |
| D. | 在水溶液中羟基和羧基均能电离出H+ |
| A. | 乙烯(乙醇) | B. | 顺丁橡胶(石油裂解气) | ||
| C. | 碘(海带) | D. | 溴(海水晒盐后的余液) |
| A. | Na3PO4 | B. | Na4P2O7 | ||
| C. | Na4P2O7 和Na5P3O10 | D. | Na3PO4、Na4P2O7和Na5P3O10 |
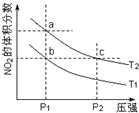 反应2NO2(g)?N2O4(g)+57kJ,若保持气体总质量不变.在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法正确的是( )
反应2NO2(g)?N2O4(g)+57kJ,若保持气体总质量不变.在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法正确的是( )| A. | a、c两点气体的颜色:a浅,c深 | |
| B. | a、c两点气体的平均相对分子质量:a>c | |
| C. | b、c两点的平衡常数:Kb=Kc | |
| D. | 状态a通过升高温度可变成状态b |
