题目内容
8.下列说法中,正确的是( )| A. | 活化分子间的碰撞一定是有效碰撞 | |
| B. | 其他条件相同时,增大反应物浓度,反应物中活化分子的百分数增加 | |
| C. | 焓变和熵变都与反应的自发性有关,它们都能独立地作为自发性的判据 | |
| D. | 常温下,FeCl3溶液中由水电离出的c (H+)一定大于1×10-7mol/L |
分析 A.活化分子发生碰撞时,只有适当的取向时,才能发生有效碰撞,才能发生化学反应;
B.增大反应物浓度,活化分子数目增多;
C.焓变和熵变判断反应的自发性,单独使用不准确;
D.常温下,水电离的c (H+)=1×10-7mol/L,氯化铁水解促进水的电离.
解答 解:A.活化分子发生碰撞时,只有适当的取向时,才能发生有效碰撞,故A错误;
B.其他条件相同时,增大反应物浓度,反应物中活化分子的数目增加,故B错误;
C.焓变和熵变都与反应的自发性有关,不能独立地作为自发性的判据,可利用综合判据△H-T△S来判断,故C错误;
D.常温下,水电离的c (H+)=1×10-7mol/L,氯化铁水解促进水的电离,则FeCl3溶液中由水电离出的c (H+)一定大于1×10-7mol/L,故D正确;
故选D.
点评 本题考查较综合,涉及反应速率影响因素、反应进行的方向及盐类水解等,注重高频考点的考查,把握相关反应原理为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
18.下列元素中,最高正价最高的是( )
| A. | 碳 | B. | 氮 | C. | 氧 | D. | 氟 |
16.下列无色透明的溶液中能大量共存的离子组是( )
| A. | Cu2+、OH-、Al3+、NO3- | B. | H+、CO32-、[Al(OH)4]-、Na+ | ||
| C. | [Al(OH)4]-、OH-、Na+、Cl- | D. | Ba2+、Mg2+、NO3-、SO42- |
13.已知:2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ/mol,下列说法不正确的是( )
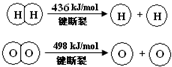

| A. | 该反应原理可用于设计氢氧燃料电池 | |
| B. | 破坏1 mol H-O键需要的能量是463.4 kJ | |
| C. | H2O(g)═H2(g)+$\frac{1}{2}$O2(g)△H=+241.8 kJ/mol | |
| D. | H2(g)中的H-H键能比H2O(g)中的H-O键能大 |
20.下列各组顺序的排列正确的是( )
| A. | 原子半径:Br<Cl<F | B. | 热稳定性:HCl<H2S<PH3 | ||
| C. | 酸性强弱:H2SiO4<H2CO3<H3PO4 | D. | 沸点:乙酸>乙醇>乙烷 |
17.下列说法正确的是( )
| A. | 仅由非金属元素不可能形成离子化合物 | |
| B. | 构成分子的粒子一定含有共价键 | |
| C. | 离子化合物中可能含有共价键 | |
| D. | 凡是有化学键断裂过程一定发生了化学反应 |
18.在允许加热的条件下,只用一种试剂就可以鉴别氯化钾、碳酸钾、偏铝酸钾、氢氧化钾、氢氧化钡、氯化钡6种溶液,这种试剂是( )
| A. | H2SO4 | B. | (NH4)2SO4 | C. | NH3•H2O | D. | NH4HSO4 |
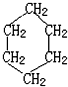 ,名称是环己烷
,名称是环己烷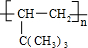 .
.