题目内容
6.在120℃时,某烃和过量O2在一密闭容器中完全反应,测知反应前后的压强没有变化,则该烃可能是( )| A. | C2H2 | B. | C3H6 | C. | C7H8 | D. | C2H4 |
分析 在120℃时水是气态,在120℃时某烃和过量O2在一密闭容器中完全反应,测知反应前后的压强没有变化,说明反应前后气体体积之和不变,则反应前后气体计量数之和不变,据此判断烃.
解答 解:在120℃时水是气态,在120℃时某烃和过量O2在一密闭容器中完全反应,测知反应前后的压强没有变化,说明反应前后气体体积之和不变,则反应前后气体计量数之和不变,
设烃的分子式为CxHy,发生的反应为CxHy+(x+$\frac{y}{4}$)O2$\stackrel{点燃}{→}$xCO2+$\frac{y}{2}$H2O,反应前后气体体积之和不变、计量数之和不变,所以1+x+$\frac{y}{4}$=x+$\frac{y}{2}$,y=4,符合条件的只有乙烯,故选D.
点评 本题考查化学方程式有关计算,明确反应前后气体计量数之和不变是解本题关键,根据方程式分析解答,题目难度不大.

练习册系列答案
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案
相关题目
17.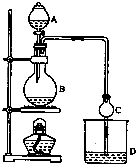 某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中放有浓硫酸,B中放有乙醇、无水醋酸钠,D中放有饱和碳酸钠溶液.已知:
某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中放有浓硫酸,B中放有乙醇、无水醋酸钠,D中放有饱和碳酸钠溶液.已知:
①无水氯化钙可与乙醇形成难溶于水的CaCl2•6C2H5OH
②有关有机物的沸点:
请回答:
(1)浓硫酸的作用是酸性、催化剂、脱水剂;若用同位素18O示踪法确定反应产物水分子中氧原子的提供者,写出能表示18O位置的化学方程式:CH3CO18OH+CH3CH2OH$?_{△}^{浓硫酸}$CH3COOC2H5+H218O.
(2)球形干燥管C的作用是防止倒吸、冷凝.若反应前向D中加入几滴酚酞,溶液呈红色,反应结束后D中的现象是溶液分层,上层无色油体液体,下层溶液颜色变浅.
(3)采用分液(操作名称)法从 D中分离出的乙酸乙酯中常含有一定量的乙醇、乙醚和水,然后加入无水氯化钙,分离出乙醇;再加入(从下列选项中选择)C,然后进行蒸馏,收集77℃左右的馏分,以得较纯净的乙酸乙酯.
A.五氧化二磷 B.碱石灰 C.无水硫酸钠 D.生石灰.
 某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中放有浓硫酸,B中放有乙醇、无水醋酸钠,D中放有饱和碳酸钠溶液.已知:
某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中放有浓硫酸,B中放有乙醇、无水醋酸钠,D中放有饱和碳酸钠溶液.已知:①无水氯化钙可与乙醇形成难溶于水的CaCl2•6C2H5OH
②有关有机物的沸点:
| 试剂 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
| 沸点/℃ | 34.7 | 78.5 | 118 | 77.1 |
(1)浓硫酸的作用是酸性、催化剂、脱水剂;若用同位素18O示踪法确定反应产物水分子中氧原子的提供者,写出能表示18O位置的化学方程式:CH3CO18OH+CH3CH2OH$?_{△}^{浓硫酸}$CH3COOC2H5+H218O.
(2)球形干燥管C的作用是防止倒吸、冷凝.若反应前向D中加入几滴酚酞,溶液呈红色,反应结束后D中的现象是溶液分层,上层无色油体液体,下层溶液颜色变浅.
(3)采用分液(操作名称)法从 D中分离出的乙酸乙酯中常含有一定量的乙醇、乙醚和水,然后加入无水氯化钙,分离出乙醇;再加入(从下列选项中选择)C,然后进行蒸馏,收集77℃左右的馏分,以得较纯净的乙酸乙酯.
A.五氧化二磷 B.碱石灰 C.无水硫酸钠 D.生石灰.
14.分别处于元素周期表第2、3周期的主族元素A和B,它们离子的核外电子层相差两层.已知A处于第m族,B处于第n族,且A只有正化合价.则A、B两元素的原子序数分别为( )
| A. | m、n | B. | m-2、10-n | C. | m+2、n+10 | D. | m+8、n+10 |
1.下表是Na、Mg、Si、S、Br五种元素的单质的沸点,其中b、e均是热和电的良导体.
(1)a的元素在元素周期表中的位置为第四周期第ⅦA族.
(2)写出d的元素原子的电子式 ;其最高价氧化物形成的晶体为原子晶体(填类型),d单质溶于强碱的离子方程式为Si+2OH-+H2O=SiO32-+2H2↑.
;其最高价氧化物形成的晶体为原子晶体(填类型),d单质溶于强碱的离子方程式为Si+2OH-+H2O=SiO32-+2H2↑.
(3)c与氢形成的分子X的空间构型为V型;写出X的水溶液与足量b元素的最高价氧化物对应水化物反应的离子方程式H2S+2OH-=S2-+H2O.
(4)上述元素所能形成的简单离子中半径最小的是Mg2+(填离子符号),最高价氧化物对应水化物酸性最强的是HBrO4(填分子式),e元素与N元素形成化合物的电子式为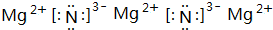 .
.
(5)b元素与氯元素形成的化合物Y的晶体中,1个晶胞内含有的基本微粒及个数是4个Na+、4个Cl-.
| 单质 | a | b | c | d | e |
| 沸点(℃) | 58.8 | 882.9 | 444.7 | 2 355 | 1 107 |
(2)写出d的元素原子的电子式
 ;其最高价氧化物形成的晶体为原子晶体(填类型),d单质溶于强碱的离子方程式为Si+2OH-+H2O=SiO32-+2H2↑.
;其最高价氧化物形成的晶体为原子晶体(填类型),d单质溶于强碱的离子方程式为Si+2OH-+H2O=SiO32-+2H2↑.(3)c与氢形成的分子X的空间构型为V型;写出X的水溶液与足量b元素的最高价氧化物对应水化物反应的离子方程式H2S+2OH-=S2-+H2O.
(4)上述元素所能形成的简单离子中半径最小的是Mg2+(填离子符号),最高价氧化物对应水化物酸性最强的是HBrO4(填分子式),e元素与N元素形成化合物的电子式为
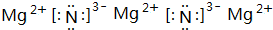 .
.(5)b元素与氯元素形成的化合物Y的晶体中,1个晶胞内含有的基本微粒及个数是4个Na+、4个Cl-.
18.下列微粒中,既含有离子键又含有共价键的是( )
| A. | NH3 | B. | NH4Cl | C. | H2S | D. | KCl |
15.下列各反应的化学方程式中,属于水解反应的是( )
| A. | H2CO3+H2O?H3O++HCO3- | B. | HCO3-+H2O?OH-+H2CO3 | ||
| C. | HCO3-+OH-?H2O+CO32- | D. | HCO3-+H2O?H3O++CO32- |
 联合国气候变化大会于2009年12月7-18日在哥本哈根召开.中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~45%.
联合国气候变化大会于2009年12月7-18日在哥本哈根召开.中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~45%.