题目内容
15.下列各反应的化学方程式中,属于水解反应的是( )| A. | H2CO3+H2O?H3O++HCO3- | B. | HCO3-+H2O?OH-+H2CO3 | ||
| C. | HCO3-+OH-?H2O+CO32- | D. | HCO3-+H2O?H3O++CO32- |
分析 水解反应的实质是:弱酸根离子或弱碱根离子离子和水电离出的氢离子或氢氧根离子结合生成弱电解质的过程,水解方程式用可逆号.
解答 解:A、碳酸是弱酸存在电离平衡分步电离,生成氢离子和碳酸氢根离子,故A错误;
B、碳酸氢根离子和水电离出的氢离子结合生成碳酸,同时生成氢氧根离子,所以属于盐类水解,故B正确;
C.方程式表示碳酸氢根离子与氢氧根离子反应生成碳酸根与水,故C错误;
D.HCO3-+H2O?H3O++CO32-是碳酸氢根离子电离出氢离子与水分子结合生成水合氢离子和碳酸根离子,属于电离方程式,故D错误;
故选B.
点评 本题考查学生对水解反应原理的理解,难度不大,注意从概念把握,识记常见的弱根离子.

练习册系列答案
 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案
相关题目
6.在120℃时,某烃和过量O2在一密闭容器中完全反应,测知反应前后的压强没有变化,则该烃可能是( )
| A. | C2H2 | B. | C3H6 | C. | C7H8 | D. | C2H4 |
3.短周期元素的离子aW2+、bX+、cY2-、dZ-具有相同的电子层结构,下列判断正确的是( )
| A. | 质子数a>b>c>d | B. | 离子的还原性Y2->Z- | ||
| C. | 氢化物的稳定性H2Y>HZ | D. | 元素的金属性:W>X |
10.下列各组物质中,用分液漏斗可以将其分开的是( )
| A. | 甲苯和苯酚 | B. | 乙醇和乙醛 | C. | 硝基苯和水 | D. | 乙酸和乙酸乙酯 |
15.含有4个原子核,10个电子的微粒是( )
| A. | CH4 | B. | NH4+ | C. | H3O+ | D. | PH3 |
 (s)+O2(g)=CO2(g)△H1 C(s)+1/2O2(g)=CO(g)△H2
(s)+O2(g)=CO2(g)△H1 C(s)+1/2O2(g)=CO(g)△H2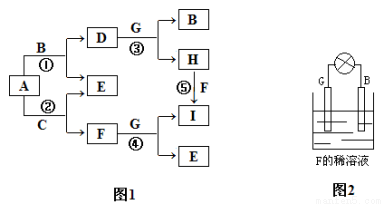
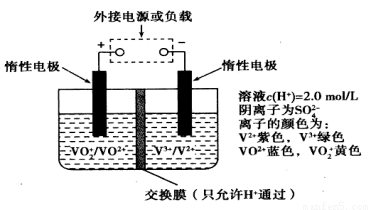
 1023个,左槽溶液中n(H+)增加了0.5mol
1023个,左槽溶液中n(H+)增加了0.5mol