题目内容
7.金属钠久置空气中发生变质,欲证明所得固体中既含有NaOH又含有Na2CO3,可以选择的操作步骤有:①固体溶解
②过滤
③加入过量BaCl2溶液
④加入过量CuCl2溶液
⑤加入足量盐酸
⑥滴加无色酚酞试液.你认为最可行的方案是( )
| A. | ①③②⑤ | B. | ①④②⑤ | C. | ①③②⑥ | D. | ①⑥⑤ |
分析 碳酸钠与盐酸反应生成气体,与氯化钡反应生成白色沉淀,可利用与盐酸或与氯化钡的反应来检验,且同时检验NaOH,利用其碱性使指示剂变色可检验,为不干扰NaOH的检验,先利用氯化钡检验碳酸钠,再利用酚酞检验NaOH,以此来解答.
解答 解:证明所得固体中既含有NaOH又含有Na2CO3,需要的步骤分别为
①固体溶解,
③加入过量BaCl2溶液(生成白色沉淀,可检验Na2CO3),
②过滤,
⑥滴加无色酚酞试液(溶液变红,可检验NaOH),
故选C.
点评 本题考查物质的检验,为高频考点,把握物质的性质、发生的反应及现象与结论的关系为解答的关键,侧重分析与实验能力的考查,注意检验时排除干扰因素,题目难度不大.

练习册系列答案
相关题目
2.下列有关氧化还原反应的叙述正确的是( )
| A. | 粮食酿酒经历淀粉→葡萄糖→乙醇,每一步均发生氧化还原反应 | |
| B. | 具有氧化性的物质在氧化还原反应中一定作氧化剂 | |
| C. | 在某些反应中可能所有元素的化合价都发生变化 | |
| D. | 单质甲能从盐溶液中置换出单质乙,单质甲一定发生氧化反应 |
12.下列说法正确的是( )
| A. | 离子键就是使阴、阳离子结合成化合物的静电引力 | |
| B. | 所有金属与所有非金属原子之间都能形成离子键 | |
| C. | 配位键在形成时,由成键双方各提供一个电子形成共用电子对 | |
| D. | 金属键的实质是金属中的“自由电子”与金属阳离子形成的一种强烈的相互作用 |
19.化学与生产、生活、社会密切相关,下列叙述错误的是( )
| A. | 食品保鲜膜、一次性食品袋的主要成分是聚氯乙烯 | |
| B. | 工业燃煤中加入适量的生石灰能有效减少二氧化硫的排放量 | |
| C. | 若同时使用硫酸亚铁和氯气处理水,能达到消毒杀菌和除去悬浮杂质的目的 | |
| D. | 航天服的主要成分是碳化硅、陶瓷和碳纤维,它们都属于无机非金属材料 |
16.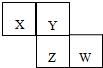 X、Y、Z、W为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子是内层电子数的3倍,下列说法正确的是( )
X、Y、Z、W为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子是内层电子数的3倍,下列说法正确的是( )
 X、Y、Z、W为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子是内层电子数的3倍,下列说法正确的是( )
X、Y、Z、W为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子是内层电子数的3倍,下列说法正确的是( )| A. | 原子半径:W>Z>X | |
| B. | 非金属性:Z>Y | |
| C. | 最高化合价:Z>X | |
| D. | 最高价氧化物对应水化物的酸性:W>Z |
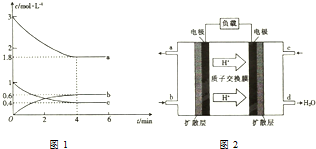 甲醇是一种低碳能源,在全球能源危机和环境污染的背景下具有良好的发展前景,在催化剂作用下可用H2(g)+CO(g)$\stackrel{催化剂}{?}$CH3OH(g),三种物质的物质的量浓度随时间变化的关系如图1所示.
甲醇是一种低碳能源,在全球能源危机和环境污染的背景下具有良好的发展前景,在催化剂作用下可用H2(g)+CO(g)$\stackrel{催化剂}{?}$CH3OH(g),三种物质的物质的量浓度随时间变化的关系如图1所示.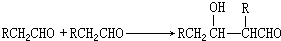
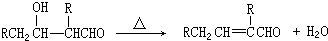

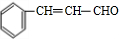 ;
;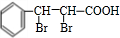 +2NaOH$→_{△}^{乙醇}$
+2NaOH$→_{△}^{乙醇}$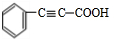 +2NaBr+2H2O
+2NaBr+2H2O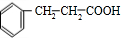 +
+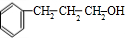 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$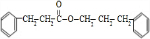 +H2O.
+H2O.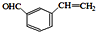 、
、 、
、
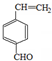 .
.